Версия для печати темы
Нажмите сюда для просмотра этой темы в обычном формате
Форум врачей-аспирантов _ Внутренние болезни _ Нецирротическая портальная гипертензия и связанные с ней заболевания печени
Автор: Ocean_ovna 6.08.2019 - 13:41
"Lasciate ogni speranza, voi ch'entrate" ("Божественная комедия" Данте Алигьери)
Здравствуйте уважаемые коллеги, особенно гепатологи, гастроэнтерологи, патоморфологи и трансплантологи!
Хочу привлечь ваше внимание и предложить для обсуждения тему, которой практически не уделяется внимания в отечественной медицинской литературе, это - Нецирротическая портальная гипертензия (Non-cirrhotic portal hypertension (NCPH)) и связанные с ней заболевания печени, такие как Узловая регенеративная гиперплазия печени (Nodular regenerative hyperplasia (NRH)), Нецирротический портальный фиброз (Noncirrhotic portal fibrosis (NCPF)) и Неполный септальный цирроз (Incomplete septal cirrhosis (ISC).
По мнению многих зарубежных экспертов эти состояния гораздо чаще встречаются, чем диагностируются ввиду объективных трудностей клинической и морфологической диагностики.
Спектр причин приводящих к этим состояниям самый разнообразный - это и наследственный фактор (описание семейного случая в прикрепленном файле), хронические вирусные гепатиты, хронические заболевания желудочно-кишечного тракта, целиакия, токсические влияния на печень, в том числе алкоголь!, ВИЧ и последствия антиретровирусной терапии, системные заболевания и др. Последствия для пациента не менее драматичные чем при циррозе, хотя есть сообщения о возможности обратного развития процесса у молодых пациентов и при начальных проявлениях заболевания . В поисках причины, при невыраженных проявлениях пациенты могут долго и безуспешно обращаться к врачам общей практики, гастроэнтерологам (в связи с метеоризмом, болями в подвздошных областях живота, чередованием поносов и запоров может выставляться ошибочный диагноз СРК (синдром раздраженного кишечника)), гепатологам и врачам других специальностей, в том числе психиатрам и дерматологам. Хотя еще со средних веков хорошо известно, что "Не следует множить сущее без необходимости" (Бритва Оккама). К сожалению, врачи плохо информированы об этих патологиях (вероятно, вообще не информированы), а соответственно у них нет настороженности в плане их диагностического поиска и в качестве дифференциального диагноза они вообще не рассматриваются.
Ниже хочу изложить свои короткие выводы по изученной зарубежной медицинской литературе.
Автор: Ocean_ovna 6.08.2019 - 15:24
В патогенезе этих заболеваний рассматривается ведущая роль облитерирующей венопатии терминальных вен печени, которая приводит к узловой регенеративной гиперплазии, нецирротическому портальному фиброзу и неполному септальному циррозу. В клинической картине могут доминировать симптомы портальной гипертензии и/или проявления хронической печеночной недостаточности вплоть до терминальных стадий с развитием печеночной комы. Трансформации в цирроз не происходит!, по крайней мере в литературе доказанных случаев такой трансформации, путем изучения серийных биопсий, не описано. Поэтому "выжидать" от пациента цирротических изменений в печени нереально. Их не будет. Пациент умрет из-за других причин связанных с прогрессированием хронической печеночной недостаточности. По сравнению с циррозом у таких пациентов статистически чаще встречаются кровотечения из варикозно расширенных вен пищевода (ВРВП). Диагностика затруднена из-за малоинформативности стандартных методов обследования. Общеклинические анализы, УЗИ, КТ, МРТ могут быть неинформативными. Врача общей практики натолкнуть на диагностический поиск у пациента этой патологии должны наличие у пациента в анамнезе гепатотоксических факторов или связанной соматической патологии, "печеночные" неспецифические жалобы, такие как умеренная болезненность в правом подреберье, метеоризм и боли в животе,розацеа носо-губного треугольника, телеангиоэктазии на лице и верхней части туловища (в том числе точечные телеангиоэктазии характерные для алкогольных поражений печени, известные как симптом Жильбера-Ано (Gilbert-Hanot symptom), галлитоз, светлый стул, чередование поносов и запоров, кожные изменения в виде розацеа, ксантомы и ксантелазмы на веках, покраснение ладоней (пальмарная эритема), гинекомастия у мужчин, изменения ногтей (ногти Терри). Описаны в литературе длительные рецидивирующие артриты в области плече-лопаточных сочленений как у пациентов с циррозом так и у пациентов с этими патологиями. Давно описано, что у пациентов с хронической печеночной недостаточностью кожа становится более пигментированной по мере ее прогрессирования, особенно открытых участков. Поэтому важен общий осмотр кожи пациента и особенно тех зон кожи, которые не подвергаются инсоляции, чтобы не списывать все на "загар". Возможна немотивированная потеря веса за относительно короткий период времени (не связанная с диетой и физическими нагрузками). При прогрессировании хронической печеночной недостаточности может отмечаться повышенная утомляемость, дневная сонливость, бессонница - из-за чего они могут становиться пациентами психиатров и отделений пограничных состояний. Трансаминазы, билирубин и другие биохимические показатели "печеночной панели" могут находится в пределах референсных значений или быть умеренно повышенными даже при развитии терминальной печеночной недостаточности, так как синтетическая функция печени долго остается сохранной.
В этом месте, хотелось бы еще раз обратить внимание, особенно молодых и начинающих врачей, в "святую веру" информативности показателей АлАТ и АсАТ для функциональной оценки печени. Эти показатели отражают процесс цитолиза в режиме "реального времени" и практически бесполезны для оценки степени хронической печеночной недостаточности при которой могут быть незначительно повышенными или "нормализоваться" при ее усугублении за счет уменьшения функционирующей паренхимы печени. Уровень аминотрансфераз в сыворотке мало зависит от патогистологических изменений в печени и может оставаться в пределах нормы, в том числе и при циррозе печени, а также может меняться спонтанно или в ответ на различные факторы, не имеющие отношения к течению заболевания. Уровни аминотрансфераз не отражают изменений гистологической структуры в печени и не имеют прогностической значимости!. Трансаминаземия при сопутствующем гепатите свидетельствует об его активности.
Может отмечаться повышенный уровень аммиака в крови. Фиброэластография (фиброскан) не выявляет фиброз (F0), или выявляет умеренный фиброз (F1-F2).. Еще одно "святое" изобретение современной медицины. Хочется напомнить, что "Фиброскан" разработан и валидирован для диагностики степени фиброза при гепатите С. Определение степени фиброза при других заболеваниях печени при помощи Фиброскана все еще в процессе исследования. Он практически бесполезен для диагностики нецирротического портального фиброза и неполного септального цирроза. Для отбора "подозрительных" пациентов предлагается https://link.springer.com/article/10.1007%2Fs00535-012-0703-z. (кликабельно) Хотя диапазон отсечения кПа по селезенке пока дискутируется, однако значительное превышение плотности селезенки над плотностью печени должны натолкнуть врача на дальнейший поиск этой патологии. (Хочу отметить, что увеличение селезенки описывается далеко не во всех случаях, даже при алкогольном циррозе).
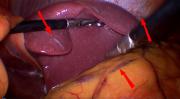
При лапароскопии определяется малоизмененная или незначительно узловатая печень с утолщенной капсулой, на поверхности печени определяются "лапчатые" фиброзы, расширенные вены сальника и париетальной брюшины. Размеры печени могут быть как слегка увеличенными, так и нормальными или уменьшенными.
Единственным достоверным методом диагностики, по мнению ряда авторов, является операционная краевая биопсия печени, так как пункционная трепанобиопсия может быть неинформативной. Кроме стандартных окрасок на соединительную ткань (по Массону, Маллори, Ван Гизон) гистологические препараты для правильной интерпретации должны быть окрашены на ретикулин. Морфологическая диагностика показывает отсутствие цирроза, умеренный портальный фиброз с незначительной инфильтрацией, расширенные синусоиды, перипортальные шунтирующие сосуды, расширенные центральные вены, мелкие узелки гепатоцитов не окруженные фиброзными тяжами, с гипертрофией в центре и атрофией по периферии. Гепатоциты в пределах узелков расположены в виде пластин толщиной 1-2 клетки. Определяются двуядерные гепатоциты. В некоторых портальных трактах может не определяться портальная вена. Нарушено взаиморасположение портальных трактов по отношению друг к другу и к центральным венам. При неполном септальном циррозе определяются тонкие соединительно-тканные прерывистые септы вокруг узелков гепатоцитов или отходящие от портальных трактов, часто слепо заканчивающиеся в паренхиме. Они лучше определяются при окраске на ретикулиновые волокна. Очень часто эксплантированные печени показывают одновременное наличие всех описываемых морфологических изменений. Неполный септальный цирроз по исследованию проведенному в Бельгии встречается приблизительно в 1% проведенных биопсий печени. По результатам центра в Бразилии в 10% случаев всех биопсий печени.
Лечение этих состояний помимо общетерапевтических подходов и контроля портальной гипертензии, может потребовать ортотопической трансплантации (ОТП) печени при развитии терминальной печеночной недостаточности. По опубликованному отчету за 20 лет ОТП проведенным в центрах трансплантации печени в Нидерландах пациентам с узловой регенеративной гиперплазией печени (NRH), стандартная шкала MELD для определения очередности трансплантации этим пациентам не подходит, так как дает более низкие значения (8-23 балла) по сравнению с пациентами с циррозом. Одно из предложений для дальнейших исследований - определить смертность среди пациентов с НРГ, находящихся в списке ожидания трансплантации печени (хотя, вероятность того, что многие из этих пациентов даже не проходят первичный отбор для внесения в список ожидания ТП очень высока. Вероятнее всего большинству из них даже пункционная биопсия печени не проводится, не говоря уже о лапароскопической. Единицам выставляется прижизненный диагноз при определенной настойчивости и настороженности врача и гепатопатолога в поиске печеночных проблем у пациента), чтобы оправдать изменение оценки MELD для пациентов с НРГ. ("Поскольку MELD имеет ряд ограничений, необходимо помнить о пациентах с заболеваниями печени, требующими ТП, тяжесть которых невозможно описать с помощью MELD. Таким пациентам эксперты дают другой приоритет". "ТПможет быть выполнена любому пациенту с терминальной стадией поражения печени, которому она продлит жизнь или улучшит ее качество (КЖ)." (Клинические рекомендации EASL:*трансплантация печени.))
Ссылка на оригинал статьи по трансплантациям печени у пациентов с узловой регенеративной гиперплазией печени проведенным в Нидерландах за 20 летний период https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5548351/ (кликабельно)
Подробный разбор клинического случая пациента с Нецирротической портальной гипертензией на русском языке в прикрепленном файле 7-го сообщения этой темы.
 Incomplete_septal_cirrhosis_an_enigmatic_disease.pdf ( 95,75 килобайт )
: 1173
Incomplete_septal_cirrhosis_an_enigmatic_disease.pdf ( 95,75 килобайт )
: 1173 Progression_idiopathic_portal_hypertension_to_incomplete_septal_cirrhosis.pdf ( 324,65 килобайт )
: 1093
Progression_idiopathic_portal_hypertension_to_incomplete_septal_cirrhosis.pdf ( 324,65 килобайт )
: 1093 Liver_Failure_and_the_Need_for_Transplantation_in_6_Patients_With_Hepatoportal_Sclerosis.pdf ( 852,35 килобайт )
: 1116
Liver_Failure_and_the_Need_for_Transplantation_in_6_Patients_With_Hepatoportal_Sclerosis.pdf ( 852,35 килобайт )
: 1116 Nodular_Regenerative_Hyperplasia_Case_Report.pdf ( 258,01 килобайт )
: 1097
Nodular_Regenerative_Hyperplasia_Case_Report.pdf ( 258,01 килобайт )
: 1097 Celiac_disease_associated_with_NCPH_ENG.pdf ( 668,13 килобайт )
: 1733
Celiac_disease_associated_with_NCPH_ENG.pdf ( 668,13 килобайт )
: 1733 Idiopathic_portal_hypertension_PRESENTATION_ENG.pdf ( 1,55 мегабайт )
: 1200
Idiopathic_portal_hypertension_PRESENTATION_ENG.pdf ( 1,55 мегабайт )
: 1200 Nodular_Regenerative_Hyperplasia_Rarely_Leads_To_Liver_transplantation_20_Year_Cohort_Study_In_Dutch.pdf ( 244,41 килобайт )
: 1072
Nodular_Regenerative_Hyperplasia_Rarely_Leads_To_Liver_transplantation_20_Year_Cohort_Study_In_Dutch.pdf ( 244,41 килобайт )
: 1072 Nodular_Regenerative_Hyperplasia_Not_All_Nodules_Are_Created_Equal_ENG.pdf ( 1,74 мегабайт )
: 1173
Nodular_Regenerative_Hyperplasia_Not_All_Nodules_Are_Created_Equal_ENG.pdf ( 1,74 мегабайт )
: 1173 Liver_transplantation_for_the_treatment_of_nodular_regenerative_hyperplasi_ENG.pdf ( 345,05 килобайт )
: 1220
Liver_transplantation_for_the_treatment_of_nodular_regenerative_hyperplasi_ENG.pdf ( 345,05 килобайт )
: 1220Автор: Ocean_ovna 7.08.2019 - 00:19
Это сообщение, в большей степени, хочу адресовать патоморфологам, патологоанатомам и гистологам. К нему я прикрепляю, на мой взгляд, наиболее интересные статьи, которые удалось найти по этой теме. В них, в основном, уделено внимание морфологической диагностике внутрипеченочной портальной гипертензии и связанных с ней изменениях печени. Возможно и клиницистам их будет интересно прочитать.
По моему мнению, наиболее профессионально в Европе вопросом морфологической диагностики заболеваний печени занимаются в Отделении патологии университетской клиники г. Левен, Бельгия. Руководитель отделения профессор Таня Роскамс (Tania Roskams, MD, PhD, Head, Liver Research Unit, Department of Imaging and Pathology, KU Leuven and University Hospitals Leuven, Leuven, Belgium. email: tania.roskams@kuleuven.be)
Думаю, что при трудностях и сомнениях можно обратиться за помощью к зарубежным коллегам, которые более профессионально разбираются в этом вопросе. Тем более, что сейчас уже не обязательно передавать стекла и блоки. Можно пересылать изображение полного стекла при помощи PathologicScanner через интернет.
Еще раз хочу акцентировать внимание на том, что по выводам зарубежных экспертов, для правильной диагностики этих состояний пункционная биопсия печени часто оказывается неинформативной. Поэтому в качестве приоритета для правильной диагностики нужно рассматривать клиновидную краевую биопсию печени при лапароскопии или операционно., с обязательной окраской на ретикулиновые волокна.
В одном отчете перипортальное иммуноокрашивание гепатоцитов на альфа-1-антитрипсин было более частым в биоптатах, показывающих NRH, чем в образцах без NRH, что позволяет предположить, что это окрашивание может быть полезно для подтверждения диагноза NRH при игольной биопсии (Nakhleh and Snover 1988 г.).
Хочется отметить, что количество проводимых биопсий печени у нас мизерное по сравнению с западными странами. Врачи их назначают неохотно даже в тех случаях, когда это явно необходимо. То есть во всех сомнительных случаях, когда нужно поставить точный диагноз. Как правило, биопсии проводят уже тем пациентам, которым и без биопсии на основании совокупности клинических и лабораторных данных можно выставить правильный диагноз.
 Nodular_regenerative_hyperplasia.pdf ( 1,74 мегабайт )
: 1120
Nodular_regenerative_hyperplasia.pdf ( 1,74 мегабайт )
: 1120 Incomplete_septal_cirrhosis_histopathological_aspects.pdf ( 425,66 килобайт )
: 1114
Incomplete_septal_cirrhosis_histopathological_aspects.pdf ( 425,66 килобайт )
: 1114 Pathology_of_idiopathic_non_cirrhotic_portal_hypertension_1_.pdf ( 2,29 мегабайт )
: 1099
Pathology_of_idiopathic_non_cirrhotic_portal_hypertension_1_.pdf ( 2,29 мегабайт )
: 1099 Incomplete_Septal_Cirrhosis_Clinical_Aspect.pdf ( 567,49 килобайт )
: 1347
Incomplete_Septal_Cirrhosis_Clinical_Aspect.pdf ( 567,49 килобайт )
: 1347 Idiopathic_Noncirrhotic_Portal_Hypertension_An_Appraisal.pdf ( 5,04 мегабайт )
: 1141
Idiopathic_Noncirrhotic_Portal_Hypertension_An_Appraisal.pdf ( 5,04 мегабайт )
: 1141 Pathology_of_idiopathic_non_cirrhotic_portal_hypertension_RU.pdf ( 1,18 мегабайт )
: 1276
Pathology_of_idiopathic_non_cirrhotic_portal_hypertension_RU.pdf ( 1,18 мегабайт )
: 1276 Zimmermann2016_ReferenceWorkEntry_NodularRegenerativeHyperplasia.pdf ( 662,37 килобайт )
: 1723
Zimmermann2016_ReferenceWorkEntry_NodularRegenerativeHyperplasia.pdf ( 662,37 килобайт )
: 1723Автор: Ocean_ovna 7.08.2019 - 00:59
Это сообщение в большей степени адресовано врачам общей практики и пациентам.
Известно, что хроническая патология внутренних органов может приводить к изменениям со стороны кожи и ее придатков - волос и ногтей. Сейчас, к большому сожалению, врачи практически не уделяют этому внимания, полагаясь на самые современные методы обследований. Можно сказать, что "лечат анализы" а не пациента, забывая, что все самые современные методы обследований имеют определенные ограничения обусловленные чувствительностью и специфичностью, а многие аппаратные методы диагностики ограниченны опытом, внимательностью и знаниями врача, который их проводит, то есть "операторозависимы". Всем врачам хорошо известно понятие ''печеночные ладони'' или пальмарная эритема. Но, почему-то, мало кто на них обращает внимание. Никакой технической сложности в оценке этого симптома нет. Диагноз по нему не поставить, но его наличие может определить дальнейшие шаги по диагностике.
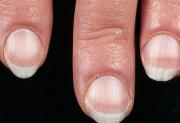
Давно описаны изменения ногтей встречающиеся при хронической патологии печени. На улицах наших городов можно часто встретить людей с белыми ногтями, но это, так сказать, крайние варианты. Здесь хочу предоставить фотографии так называемых https://www.fordevr.com/terry-nails-pictures.html (кликабельно), которые чаще всего встречаются при диффузных заболеваниях печени, особенно алкогольной этиологии. В настоящее время для диагностики ногтей Терри применяются критерии уточненные https://www.ncbi.nlm.nih.gov/pubmed/6143196 в 1984 году. Ложе ногтя может быть не только белым, но и бледно розовым с дистальной полоской от 0.5 до 3 мм., коричневого, светло-коричневого или розового цвета, лунула может как определяться, так и отсутствовать, сливаясь по цвету с ложем ногтя. Как правило, вначале более заметны изменения ногтей большого и указательного пальцев. Характерна симметричность изменений. И хотя сейчас ногти не являются диагностическим критерием, однако они могут помочь направить мысль врача по пути к установлению правильного диагноза.
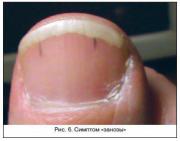
"Сплит симптом" или симптом "занозы" - тонкая вертикальная темная полоска на ногте напоминающая волосок, встречается гораздо реже.
 Terry_nails_in_a_patient_with_chronic_alcoholic_liver_disease.pdf ( 144,23 килобайт )
: 1123
Terry_nails_in_a_patient_with_chronic_alcoholic_liver_disease.pdf ( 144,23 килобайт )
: 1123 The_Diagnosis_Terry_Nails.pdf ( 145,72 килобайт )
: 1244
The_Diagnosis_Terry_Nails.pdf ( 145,72 килобайт )
: 1244Автор: Ocean_ovna 8.08.2019 - 21:40
В этом сообщении хочу уделить внимание такому, часто недиагностируемому на догоспитальном и госпитальном этапах состоянию, как минимальная и латентная печеночная энцефалопатия. Поэтому оно в большей степени адресовано врачам общей практики, невропатологам, гастроэнтерологам и гепатологам.
Устоявшиеся "стереотипы" медицины предполагают поиск симптомов энцефалопатии у пациентов с циррозом. Соответственно, описываемые заболевания автоматически необоснованно исключают пациента из диагностического поиска врачом симптомов печеночной энцефалопатии (ПЭ). Даже явные симптомы печеночной недостаточности, а соответственно ПЭ, такие как - "печеночное дыхание" (fetor hepaticus), отвращение к табаку у курильщиков, изменение запаха пота, усиленная пигментация кожи - могут трактоваться врачами у этих пациентов как "выдумки" пациента.
Как я уже писал выше, ввиду объективных трудностей лабораторной и инструментальной диагностики, пациенты часто необоснованно направляются на лечение к психиатрам и в отделения пограничных состояний, где вместо адекватного диагноза и лечения назначаются психотропные препараты, прием которых в еще большей степени усугубляет и без того нарушенную функцию печени, и как правило не приводит к улучшению самочувствия. Из психоневрологических жалоб у пациентов на первый план могут выступать повышенная утомляемость ("синдром хронической усталости", "печеночная лень"), дневная сонливость, инверсия сна, на более поздних этапах бессонница. Могут отмечаться невнимательность, забывчивость, раздражительность, иногда агрессивность, но в целом когнитивные функции сохранены. Часто пациенты-водители становятся участниками ДТП.
Иногда можно обнаружить несинхронный несимметричный латеральный тремор пальцев при разгибании кисти (аналог хорошо известного "астериксиса", можно сказать его начальные проявления).
В диагностике минимальной печеночной энцефалопатии у таких пациентов может помочь определение уровня аммиака. Большинство авторов не приходят к однозначным выводам по трактованию повышения этого показателя, так как иногда даже у пациентов с печеночной комой его уровень не повышен, а сам анализ требует соблюдения определенных условий на преаналитическом этапе и вероятно поэтому большинство отечественных лабораторий его не делают. Но возможно, в практической деятельности его повышение целесообразно рассматривать как серьезный сигнал, а отсутствие при явных "печеночных" стигмах расценивать как неинформативное. Думаю, что такой подход в практической медицине более оправдан и может принести больше пользы для конкретного пациента) в сыворотке крови (не всегда, но часто его уровень будет повышенным). Достаточно достоверным тестом для диагностики считается http://hepa-merz.ru/pechen/diagnostika/. Чувствительность теста около 70%. (Для тех, кто захочет попробовать пройти тест. Рекомендую учитывать результаты первых трех попыток, так как улучшение прохождения теста при большем количестве повторений связанно с обычной тренировкой). По данным многих наблюдений коррекция гипераммониемии препаратами лактулозы (Дюфалак) и L-орнитина L-аспартата (Гепа-Мерц), а также адекватное ограничение животного белка в рационе и отказ от алкоголя во многих случаях приводят к улучшению самочувствия, нормализации сна и улучшению показателей выполнения психометрических тестов.
Более сложные для выявления минимальной печеночной энцефалопатии, так как необходима специальная аппаратура - Тест на определение критической частоты слияния мерцания, Электроэнцефалография с вызванными потенциалами и Магнито-резонансная спектроскопия, которая считается наиболее чувствительным исследованием.
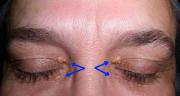
Часто пациенты с хроническими диффузными заболеваниями печени обращаются к окулистам с жалобами на сухость и жжение в глазах ("синдром сухого глаза"). Может отмечаться некоторая нечеткость зрения, усугубляющаяся по мере прогрессирования печеночной энцефалопатии (ПЭ), из-за поражения сосудов сетчатки. Также достаточно часто встречается хемоз (отек)коньюнктивы, усиливающийся по мере усугубления ПЭ и белково-энергетической недостаточности. В нескольких зарубежных работах сообщалось о развитии "корковой" слепоты у пациентов при эпизодической печеночной энцефалопатии, на поздних этапах заболеваний печени. Описаны случаи тиннитуса (звона или писка в ушах)у пациентов с печеночной энцефалопатией. Также, есть описание случаев имитирующих острое нарушение мозгового кровообращения (ОНМК) и эпилептиформные приступы у таких пациентов, а при персистирующей печеночной энцефалопатии возможна имитация симптомов паркинсонизма, так как симптомы некоторых пациентов с печеночной энцефалопатией схожи с симптомами пациентов с болезнью Паркинсона (замедленная мозговая деятельность, скованность движений, тремор). (интересно, не ошиблись ли с диагнозом https://ru.wikipedia.org/wiki/%D0%A3%D0%B8%D0%BB%D1%8C%D1%8F%D0%BC%D1%81,_%D0%A0%D0%BE%D0%B1%D0%B8%D0%BD?), о чем следует помнить врачам скорой помощи и неотложных состояний и неврологам.
Как видно из всего изложенного, очень большая роль в выявлении патологии печени возлагается на врача общей практики с которым впервые встречается пациент. От его внимательного осмотра и правильной оценки жалоб зависит правильная диагностика проблемы, а соответственно и правильное лечение. Во многих случаях отсутствие лабораторных и инструментальных изменений не должны успокаивать и останавливать врача в диагностическом поиске "печеночной" проблемы у пациента. Пройдя весь путь диагностического поиска и получив неубедительные результаты, врач должен помнить, что по выводам зарубежных экспертов, которые занимались этой проблемой - единственным достоверным методом для выявления нецирротической внутрипеченочной портальной гипертензии и связанных с ней узловой регенеративной гиперплазией печени, нецирротическим портальным фиброзом и неполным септальным циррозом на современном этапе медицины является краевая клиновидная биопсия печени
Ссылка на статью (кликабельна): https://www.med-sovet.pro/jour/article/view/1421 П. О. БОГОМОЛОВ, А. О. БУЕВЕРОВ, О. В. УВАРОВА, М. В. МАЦИЕВИЧ
Здесь можно посмотреть видеопрезентацию профессором Буеверовым О.А. https://www.youtube.com/watch?v=yXSC8FD3OZY (кликабельно), которое было проведенно у пациентов с вирусным гепатитом С и минимальным фиброзом (F1) печени.
 Rare_Case_of_Anton_Babinski_Syndrome_in_Hepatic_Encephalopathy.pdf ( 111,25 килобайт )
: 1805
Rare_Case_of_Anton_Babinski_Syndrome_in_Hepatic_Encephalopathy.pdf ( 111,25 килобайт )
: 1805 Reversible_Cortical_Blindness_with_Hepatic_Encephalopathy.pdf ( 372,67 килобайт )
: 1201
Reversible_Cortical_Blindness_with_Hepatic_Encephalopathy.pdf ( 372,67 килобайт )
: 1201 MR_Imaging_Findings_in_Hepatic_Encephalopathy.pdf ( 387,59 килобайт )
: 1484
MR_Imaging_Findings_in_Hepatic_Encephalopathy.pdf ( 387,59 килобайт )
: 1484 Number_Connection_Test_PRINT.pdf ( 11,56 килобайт )
: 1047
Number_Connection_Test_PRINT.pdf ( 11,56 килобайт )
: 1047 FOCAL_NEUROLOGICAL_SYNDROMES_IN_HEPATIC_FAILURE.pdf ( 830,29 килобайт )
: 1056
FOCAL_NEUROLOGICAL_SYNDROMES_IN_HEPATIC_FAILURE.pdf ( 830,29 килобайт )
: 1056Автор: Ocean_ovna 9.08.2019 - 07:39
"И сказал Бог: да произрастит земля зелень, траву, сеющую семя (по роду и подобию ее), и дерево плодовитое, приносящее по роду своему плод, в котором семя его на земле, и стало так. И увидел Бог, что это хорошо. Был вечер и было утро: день третий" (Библия, Ветхий Завет, Бытие)
Несмотря на такое необычное начало этого поста, хотел в нем немного написать о науке вообще и медицинской науке в частности. Может быть, в какой-то степени, применительно к предыдущим сообщениям.
Наука, безусловно, основана на формальной логике. Она не обладает абсолютным знанием. Она не претендует на абсолюты. Ее знания все время меняются, а двигают науку парадоксы. Об одном таком парадоксе я и хочу порассуждать. Известен он в науке как парадокс "https://ru.wikipedia.org/wiki/%D0%A1%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D0%BE%D1%88%D0%B8%D0%B1%D0%BA%D0%B0_%D0%B2%D1%8B%D0%B6%D0%B8%D0%B2%D1%88%D0%B5%D0%B3%D0%BE" (кликабельно) и является логической ошибкой сосредоточения внимания на людях или вещах, которые прошли через некоторый процесс отбора, и игнорирования тех, кто этого не сделал, как правило, из-за их недостаточной видимости. https://www.youtube.com/watch?v=P-6ZFcBmTAE. Это может привести к ложным выводам несколькими различными способами. Это форма предвзятости выбора. "Систематическая ошибка выжившего" может привести к чрезмерно оптимистичным убеждениям, потому что неудачи игнорируются. Другим примером особого способа предвзятого отношения к выживанию было бы думать, что инцидент не так опасен, как это было, потому что все, с кем вы общаетесь впоследствии, выжили. Даже если бы вы знали, что некоторые люди мертвы, у них не будет своего голоса, чтобы добавить к разговору, что приведет к предвзятости в разговоре.
Применительно к медицинской науке и описанным патологиям можно уверенно сказать, что незнание или игнорирование их еще не говорит о том, что их не существует. Что эти диагнозы не выставляются у нас я знаю из "первых уст". Кто имеет доступ, может проверить мои слова. Специалисты с "профессиональной гордостью" могут мне возразить, что например диагноз неполный септальный цирроз отсутствует в Международной классификации болезней (МКБ 10) и будут формально правы. Но, во первых, МКБ 10 это не догмат и не Библия, как и все, что создано в науке, она будет уточняться и изменяться и это не повод игнорировать проблему, как будто ее не существует вовсе. Во вторых, МКБ 10 достаточно гибкая классификация в которой присутствуют другие рубрики которыми можно воспользоваться для формализации. В третьих, для сомневающихся, неполный септальный цирроз входит в Морфологическую классификацию циррозов предложенную Всемирной ассоциацией гепатологов (Акапулько, 1974) и ВОЗ (1978). Думаю все же, что дело не в классификации, а в незнании и игнорировании. Наша медицина по отношению к этим патологиям находится в плену устаревших стереотипов. Прежде всего патологию не знают наши патоморфологи, соответственно ее и не диагностируют. Ведь очень просто подходить ко всему со шкалами METAVIR или Кнодель, принимая как аксиому их "универсальность", но не видеть целостной морфологической картины. Термометр отличный измерительный прибор, но спидометр автомобиля он заменить не может. Шкала в медицине ведь важна не сама по себе, она должна, в какой-то степени, быть полезна для выяснения прогноза. Значит в данном случае она не дает нам точной информации, а просто констатирует факт наличия или отсутствия фиброза. Безусловно, медицина как наука будет развиваться дальше. На многие вопросы будут получены ответы. Хотелось бы, чтобы "систематическая ошибка выжившего" была если и не исключена, то хотя бы минимизирована.
Автор: Ocean_ovna 14.08.2019 - 20:11
"Каждое утро прилетает орел и принимается за свою кровавую трапезу. За ночь заживают раны, и вновь вырастает печень, чтобы днем дать новую пищу орлу. Годы, века длятся эти муки. Истомился могучий титан Прометей, но не сломлен его гордый дух страданиями." ("Миф о Прометее". Мифы и Легенды древней Греции)
В этом сообщении, я бы хотел коротко уделить внимание одному из "орлов", терзающих печень современного общества, применительно к вышеописанным патологиям - алкоголю. К сожалению, потребление алкогольной продукции во многих странах мира населением неуклонно растет. Особенно высокие цифры отмечаются в странах бывшего СССР. Первая пятерка стран по данным 2014 года по мере убывания выглядит так: Молдова (18,22 л), Чехия (16,45 л), Венгрия (16,27 л), Россия (15,76), Украина (15,60). Данные по потреблению алкоголя за 2018 год можно посмотреть https://ru.wikipedia.org/wiki/%D0%A1%D0%BF%D0%B8%D1%81%D0%BE%D0%BA_%D1%81%D1%82%D1%80%D0%B0%D0%BD_%D0%BF%D0%BE_%D0%BF%D0%BE%D1%82%D1%80%D0%B5%D0%B1%D0%BB%D0%B5%D0%BD%D0%B8%D1%8E_%D0%B0%D0%BB%D0%BA%D0%BE%D0%B3%D0%BE%D0%BB%D1%8F_%D0%BD%D0%B0_%D1%87%D0%B5%D0%BB%D0%BE%D0%B2%D0%B5%D0%BA%D0%B0(кликабельно). Ассортимент алкогольной продукции постоянно расширяется и обновляется. Если, применительно к табачной продукции все более-менее приведено в "цивилизованные рамки" и она маркируется практически во всем мире специальными предупреждающими наклейками и яркими поучительными картинками, то в отношении алкоголя все обстоит с точностью до наоборот. На телевидении присутствует явная и скрытая реклама, а героев молодежных сериалов зачастую можно увидеть с бокалом в руке или за стойкой бара. О предупреждающих обозначениях и говорить не приходится. Обществом, алкоголь приравнен к пищевым продуктам и продается практически без ограничений, хотя по медицинским свойствам вполне относится к наркотическим веществам, вызывающим чувство эйфории, оглушенности при больших дозах, а при регулярном употреблении может вызывать зависимость. Население, как правило, зная о потенциальном риске употребления алкоголя в общем, практически не владеет количественными значениями этого риска.Ещё в 1927 году выдающийся психиатр В. М. Бехтерев писал: "К сожалению, вопросы о громадном вреде, приносимом алкоголем, недостаточно ясны для малокультурных масс, да и большинству интеллигентов не представляется очевидным, что алкоголь есть безусловный яд. Даже, наоборот, господствуют всюду мнения о полезности малых и умеренных доз алкоголя, хотя попытки некоторых учёных доказать эту "полезность" потерпели полное крушение с позднейшими научными исследованиями". По современным данным, учитывая особенности обмена этанола у определенных категорий пациентов, т.н."полиморфизм генов", http://www.euro.who.int/ru/health-topics/disease-prevention/alcohol-use/data-and-statistics/q-and-a-how-can-i-drink-alcohol-safely (кликабельно)В большинстве случаев мы не можем прогнозировать, какие потенциальные последствия может вызвать употребление алкоголя у каждого конкретного пациента. Вероятно, стоило бы задуматься о раннем генетическом скрининге на http://forum.disser.ru/index.php?showtopic=3885&st=2070 (кликабельно), который очень активно обсуждается в соседней ветке и по выводам экспертов достаточно часто встречается в популяции (около 10%, а в некоторых этнических группах до 30%)в большинстве случаев может протекать бессимптомно, тем не менее ограничивая функциональный резерв печени. В этом случае мог бы сработать принцип "предупрежден - значит вооружен".
В гепатологии хорошо и давно известен, в виду своей очевидности и "яркости" клинико-лабораторных изменений, так называемый "континуум" Алкогольной болезни печени (АБП) - от жирового гепатоза, через хронический стеатогепатит и фиброз, к циррозу печени и гепато-целлюлярной карциноме, который часто и много описывается как в зарубежных, так и отечественных руководствах и практически очень мало информации о причинной роли алкоголя для описываемых патологий, хотя упоминания об этом встречаются постоянно. Вероятную причину такой ситуации я изложил в предыдущем сообщении. Думаю, частота этих заболеваний намного выше ожидаемой. Косвенно, об этом может свидетельствовать то, что по данным отчетов, некоторым пациентам с описываемыми патологиями, которым была проведена трансплантация печени, выставлялся предтрансплантационный диагноз "алкогольный цирроз", не подтвержденный при последующем исследовании эксплантатов, но вероятно отражающий факт регулярного употребления алкоголя в анамнезе (как говорится - кому как повезет), а также то, что единственная рубрика МКБ 10 посвященная Алкогольной болезни печени, - https://mkb-10.com/index.php?pid=10332 (кликабельно) лишена опоры на морфологические изменения печени. Также, уклонение этих патологий от анализа может скрываться, например, в случаях суицида в этой категории пациентов. Вероятно, есть и другие причины. В целом, на сегодняшний момент, ситуация остается неопределенной, так как фактическая распостаненность этих патологий остается неизвестной. Выскажу предположение, что существует "альтернативный континуум" алкогольной болезни печени (АБП), с формированием первичного аффекта в виде терминальной облитерирующей венопатии и развитием узловой регенеративной гиперплазии, нецирротического портального фиброза и неполного септального цирроза, который из-за своей "неяркости" изменений клинико-лабораторных данных "скрыт" от клинициста, в отличие от "классического" цирротического процесса. Возможно, что для развития патологического процесса именно по этому пути, кроме прямого токсического влияния этанола необходимо наличие у пациента каких-либо протромботических факторов.
P.S. В этом посте прикрепляю одну из лучших, на мой взгляд, работ (может быть и единственную, напрямую к его теме не относящуюся) , которую удалось найти в "русскоязычном сегменте". Она опубликована коллективом авторов Донецкого национального медицинского университета и Украинского научно-практического центра эндокринной хирургии, трансплантации эндокринных органов и тканей (Киев) под руководством профессора Губергриц Натальи Борисовны (в настоящее время Наталья Борисовна работает в Одессе. Повезло одесситам!). Эта статья посвящена подробному клиническому разбору пациента с Нецирротической портальной гипертензией. В ней очень хорошо демонстрируется с какими трудностями может столкнуться практический врач в установлении правильного диагноза.
Здесь описание еще одного интересного http://health-ua.com/article/4734-netcirroticheskaya-portalnaya-gipertenziya-slishkom-mnogo-horoshego (кликабельно)
Автор: Ocean_ovna 17.08.2019 - 15:05
В этом сообщении, хочу уделить отдельное внимание устоявшимся медицинским "стереотипам" в отношении такого показателя биохимического анализа крови и "печеночной панели" как билирубин, применительно к описываемым патологиям. Как я уже показал, опираясь на зарубежные источники, что при этих патологиях биохимические показатели иногда могут находится в пределах нормативных или незначительно измененных значений, в том числе и билирубин, несмотря на развитие у этих пациентов выраженной печеночной недостаточности. Это хорошо продемонстрировано в работе по трансплантациям печени у пациентов с Узловой регенеративной гиперплазией проведенным в Нидерландах, ссылка на которую есть во втором сообщении этой темы.
Хорошо известнен в медицине факт, что при развитии и прогрессировании печеночной недостаточности у пациентов отмечается стойкое и прогрессирующее "обесцвечивание стула". С другой стороны, также известен и не подвергается сомнению факт того, что "обесцвеченный стул" сопровождает появление выраженной желтухи и повышение уровня билирубина в сыворотке. Выскажу свое предположение, что применительно к описываемым патологиям возможны все варианты и уровень билирубина может слабо коррелировать со степенью "посветления стула" при печеночной недостаточности у этих пациентов. К сожалению, в плену устоявшихся "стереотипов" медицины могут находится даже известные и опытные клиницисты с учеными степенями. В качастве примера такого подхода, привожу ссылку на стенограмму видеоразбора https://internist.ru/publications/detail/pacientka-s-hronicheskoy-funkcionalnoy-bolyu-v-zhivote-i-stoykim-narusheniem-trofologicheskogo-statusa/?sphrase_id=237382 (кликабельно). Несмотря на многолетние жалобы пациента на "обесцвеченный стул", изменение трофологического статуса пациента - http://bono-esse.ru/blizzard/RPP/M/GKT/trofost.html(кликабельно), снижение альбуминов в сыворотке крови, положительные серологические тесты на вирусный гепатит С (а я уже писал, что эти патологии описаны, в том числе, для хронических вирусных гепатитов), на УЗИ "печень не увеличена, контур ровный, паренхима средней эхогенности с подчеркнутыми портальными трактами, воротная вена 9,8 мм." - биопсия печени, для исключения диффузных изменений в печени, так и не была выполнена. Вместо этого жалобы пациента были переведены в "плоскость" психосоматических нарушений и мнимых субьективных преувеличений самим пациентом. Хотел выложить здесь и видео с этим разбором, которое видел на этом сайте несколько лет назад, но, к сожалению, не смог его найти.
Автор: Ocean_ovna 19.08.2019 - 14:13
В этом сообщении хотел бы уделить внимание ценности для диагностики узловой регенеративной гиперплазии, нецирротического портального фиброза и неполного септального цирроза таких неинвазивных методов исследования как - УЗИ органов брюшной полости, доплерография сосудов брюшной полости и фиброэластография печени и селезенки.
УЗИ органов брюшной полости считается малоинформативным методом исследования по отношению к этим патологиям, так как анатомические изменения печени минимальны и размеры могут приближаться к норме. Вероятнее всего, возможно обнаружить только некоторое повышение эхогенности паренхимы и ее "зернистость" той или иной степени. Если будут обнаружены увеличение диаметра воротной вены и размеров селезенки, такие признаки безусловно будут трактоваться как УЗИ признаки портальной гипертензии (хотя проведенные исследования показывают слабую статистическую связь между расширением воротной вены и портальной гипертензией, в отличие от увеличения селезенки. Но отсутствие увеличения селезенки не исключает портальную гипертензию). Но так происходит далеко не всегда. Предположу, что на это влияет скорость нарастания портальной гипертензии (вероятнее всего присутствуют и другие более сложные механизмы), если скорость незначительна, то включаются механизмы адаптации в виде увеличения плотности паренхимы селезенки и портосистемное шунтирование крови, в том числе через микрошунтирование в самой паренхиме печени.Признаками портальной гипертензии считаются увеличение диаметра воротной вены более 13 мм и замедление кровотока в ней. Согласно некоторым данным, увеличение диаметра воротной вены считается ненадежным признаком, т.к. в норме этот показатель весьма вариабелен. Необходимо также отметить, что увеличение диаметра воротной вены не является обязательным признаком, существующим постоянно. Это связано с тем, что после образования портокавальных анастомозов диаметр воротной вены может уменьшиться до нормальных величин. Скорее всего, бОльшую ценность могла бы дать доплерография сосудов брюшной полости, при которой в такой ситуации должен ускоряться кровоток в портальной системе, а именно в верхней брыжеечной вене и селезеночной вене скорость кровотока превышает значения ее в воротной вене, при этом скорость кровотока в воротной вене может быть различной в зависимости от степени диффузных изменений в печени. Соответственно, фиброскан (фиброэластография) печени давая достаточно информативные данные по отношению к степени фиброзирования печени в этом случае дает нам чересчур "оптимистическую" информацию. Как я уже писал, в нескольких зарубежных статьях, для отбора "подозрительных" на NCPH/NCPF/NRH/ISC пациентов предлагается проводить https://link.springer.com/article/10.1007%2Fs00535-012-0703-z (кликабельно). Показано, что при циррозе плотность паренхимы селезенки в какой-то степени соотносится с плотностью паренхимы печени, в отличии от нецирротической портальной гипертензии, когда плотность селезенки существенно превышает плотность печени, которая, в свою очередь, не показывает "цирротических" значений. Вероятно в большей степени "интуитивно", такие работы выполнялись и отечественными исследователями, с методологией и научными выводами которых можно дискутировать, но факт остаётся фактом, группа пациентов с превышением плотности селезёнки над плотностью печени прогностически отличается от других пациентов и очевидно это требует дальнейших исследований (статья в прикрепленном файле_RU).
 Diagnostic_possibilities_of_sonoelastography_liver_and_spleen_RU.pdf ( 320,39 килобайт )
: 1150
Diagnostic_possibilities_of_sonoelastography_liver_and_spleen_RU.pdf ( 320,39 килобайт )
: 1150 Role_of_Ultrasound_Doppler_in_Evaluation_of_Portal_Hypertension_ENG.pdf ( 562,78 килобайт )
: 1522
Role_of_Ultrasound_Doppler_in_Evaluation_of_Portal_Hypertension_ENG.pdf ( 562,78 килобайт )
: 1522 Ultrasonography_in_Portal_Hypertension.pdf ( 323,11 килобайт )
: 1105
Ultrasonography_in_Portal_Hypertension.pdf ( 323,11 килобайт )
: 1105 Hepatoportal_Sclerosis_CT_ENG.pdf ( 819,34 килобайт )
: 1067
Hepatoportal_Sclerosis_CT_ENG.pdf ( 819,34 килобайт )
: 1067 Idiopathic_portal_hypertension_ultrasound_findings_ENG_.pdf ( 600,95 килобайт )
: 1406
Idiopathic_portal_hypertension_ultrasound_findings_ENG_.pdf ( 600,95 килобайт )
: 1406 Multimodality_imaging_of_obliterative_portal_venopathy_ENG.pdf ( 2,64 мегабайт )
: 1212
Multimodality_imaging_of_obliterative_portal_venopathy_ENG.pdf ( 2,64 мегабайт )
: 1212Автор: Ocean_ovna 11.09.2019 - 16:56
В этом сообщении хочу уделить внимание такому состоянию у пациентов с диффузными заболеваниями печени как персистирующая печеночная энцефалопатия, которая в некоторых случаях не поддается стандартной терапии лактулозой, LOLA и рифаксимином. В поддержании такого состояния во многих случаях придается значение возникновению спонтанных портосистемных шунтов у пациентов. Многоцентровое Европейское когортное исследование продемонстрировало роль крупных спонтанных портосистемных шунтов при хронической затяжной или рецидивирующей ПЭ и обосновало эффективность и безопасность эмболизации этих шунтов при условии если имеется достаточный функциональный резерв печени. Как показано в статье, далеко не во всех случаях персистирующей печеночной энцефалопатии крупные портосистемные шунты обнаруживаются. Вероятно, в такой ситуации, возможность проведения ортотопической трансплантации печени (ОТП), должна быть рассмотрена в качестве приоритета.
 Diagnostic_approach_to_persistent_hepatic_encephalopathy_ENG.pdf ( 321,08 килобайт )
: 1239
Diagnostic_approach_to_persistent_hepatic_encephalopathy_ENG.pdf ( 321,08 килобайт )
: 1239 Embolization_of_Large_Spontaneous_Portosystemiс_Shunts_ENG.pdf ( 781,32 килобайт )
: 1841
Embolization_of_Large_Spontaneous_Portosystemiс_Shunts_ENG.pdf ( 781,32 килобайт )
: 1841Автор: Ocean_ovna 29.06.2020 - 22:52
Решил продублировать в этой теме http://forum.disser.ru/index.php?showtopic=3885&view=findpost&p=24494, на мой взгляд, из темы синдром Жильбера, так как она непосредственно касается обсуждаемых (к сожалению пока в виде монолога)здесь вопросов и короткие личные выводы по ней, не претендующие на строгую научность и доказательность. Работа выполнена в Индии в далеком уже 1974 году.
Ни у одного пациента с СЖ уровень прямого билирубина не достигал 8,5 мкмоль/л. Хотя выборку (3 чел) тоже репрезентативной не назовешь. При НЦПФ уровень прямого билирубина был в некоторых случаях несколько выше чем при СЖ, но общий билирубин был в норме. При НЦПФ 10 дневный курс фенобарбитала (180мгх2раза в день) существенно повышал активность УДФ-ГТ даже по сравнению с СЖ. Безбелковая диета у крыс достоверно снижала активность УДФ-ГТ
Какие бы я сделал выводы:
1. Фенобарбиталовый тест не подходит для дифференциальной диагностики СЖ и НЦПФ.
2. Повышенный уровень прямого билирубина при СЖ требует дифференциальной диагностики с другими заболеваниями печени, в том числе с НЦПФ.
3. При сочетанной патологии СЖ+НЦПФ может повышаться как прямой (НЦПФ) так и непрямой(СЖ) билирубин, который будет снижаться на фоне приема фенобарбитала.
4. Для предварительного отбора пациентов на биопсию с целью диагностики НЦПФ наряду с клиническими данными, может быть использована эластометрия печени и селезенки.
Автор: Lara 2.07.2020 - 14:19
Добрый день! Ocean_ovna! Решила все-таки здесь задавать вопросы, а на форуме с Синдромом Жильбера будем про него, родимого, писать)))
Вашу историю знаю по тому форуму. Если бы Вы чуть раньше у себя диагностировали то, что поняли сейчас - какую тактику бы выбрали? Гепатопротекторы, какие, гептрал? Или просто Гепа-мерц? Лактулоза? Диета понятно, алкоголь тоже, а что еще?
Если все говорят - анализы нормальные, а ладони и ногти и нарушения сна - этого в упор не видят)
И еще - урсодезоксихолевую кислоту же при этих делах нельзя, я так понимаю? а я полгода на ней просидела, и отменить боюсь, и пить боюсь)
Автор: Ocean_ovna 2.07.2020 - 23:33
Вашу историю знаю по тому форуму. Если бы Вы чуть раньше у себя диагностировали то, что поняли сейчас - какую тактику бы выбрали? Гепатопротекторы, какие, гептрал? Или просто Гепа-мерц? Лактулоза? Диета понятно, алкоголь тоже, а что еще?
Если все говорят - анализы нормальные, а ладони и ногти и нарушения сна - этого в упор не видят)
И еще - урсодезоксихолевую кислоту же при этих делах нельзя, я так понимаю? а я полгода на ней просидела, и отменить боюсь, и пить боюсь)
Добрый день, Lara. Спасибо, что обратили внимание на эту тему, посвященную малоизвестной, практически недиагностируемой отечественной медициной, но отнють не значит, что редкой патологии.
Опыт применения УДХК несколько лет назад у меня был. Прошел УЗИ с эластографией у одного из лучших специалистов - фиброза тогда небыло вовсе, печень в норме, небольшая взвесь в желчном, вот и решил попробовать. После первых приемов просто "летал", бодрость, свободное носовое дыхание, как будто открыли перекрытые трубы. Правда, через некоторое время этот эффект прошел, но тем не менее билирубин незначительно повышенный снизился до нормы. К сожалению, одним из противопоказаний к приему УДХК, указанным в инструкции, является печеночная недостаточность, а вот печеночной "достаточностью" я свои симптомы при всем желании назвать не могу), поэтому и остерегаюсь принимать ее .
Что бы сделал? Тогда у меня еще небыло тех знаний, которые есть сейчас))). Если бы были, то вероятно, кроме общих мероприятий, о которых вы упомянули, ограничил бы животный белок (всегда был мясоедом), однозначно лактулоза, гепа-мерц и скорее всего внутривенно курсами препараты глицирризиновой кислоты - по ней достаточно хорошие данные при фиброзе, а он, хоть и минимальный, но все же имеется и вполне естественно,что его наличие, вероятнее всего, может ухудшать клинические проявления. Другим перспективным антифибротическим препаратом может оказаться мелатонин. Согласно обзору опубликованному в 2018 в журнале Nutrients было показано, что добавление мелатонина в дозе 10 мг / день значительно увеличивает уровень мелатонина в плазме и снижает ферменты печени. Исследователи показали, что добавление мелатонина может улучшить функцию митохондрий печени и снизить окислительный стресс. Мелатонин в гепатоцитах играет защитную роль в отношении митохондриальной дисфункции и помогает инактивировать фиброгенез.
PS. Скорее всего, на ранних стадиях, если гипотетически предположить, что удалось поставить правильный диагноз, уместно назначение антикоагулянтов, так как ведущая роль в патогенезе этих состояний отводится облитерирующей венопатии терминальных вен. Также целесообразно с патогенетической точки зрения применение неселективных бета-блокаторов (карведилол, пропранолол)с целью уменьшения портального давления. Думаю, это не только приводит к профилактике кровотечений из варикозно-расширенных вен пищевода (о чем все пишут), но и в целом улучшает портальную гемодинамику, вероятно уменьшая скорость прогрессирования заболевания, хотя и возможность гепатотоксичности препаратов сбрасывать со счетов нельзя, поэтому необходим периодический контроль хотя-бы маркеров цитолиза (АЛТ/АСТ).
Если все говорят - анализы нормальные, а ладони и ногти и нарушения сна - этого в упор не видят)
Гораздо хуже то, что в упор не видят имеющихся морфологических изменений после нескольких биопсий, в том числе клиновидной при лапароскопии, а это уже грустно и свидетельствует о том, что эту патологию не знают, считая редкой просматривают и скольким пациентам не выставляется правильный диагноз тот еще вопрос и если такое происходит, то это может быть распостраненной проблемой.
Автор: Ocean_ovna 30.11.2020 - 00:29
Еще один интересный отчет по узловой регенеративной гиперплазии (NRН)печени у пациента 47 лет, которому была выполнена ортотопическая трансплантация печени с предтрансплантационным диагнозом "цирроз печени". При поступлении в больницу для оценки возможности трансплантации состояние пациента было оценено как тяжелое. У него имелась общая отечность с асцитом, элементы гинекомастии, атрофия яичек, и спленомегалия с нижним краем селезенки на 5см ниже реберной дуги. У него небыло желтухи и сосудистых "паучков". Концентрация билирубина составила 24 мкмоль / л (диапазон 0-18), альбумин 26 г / л (диапазон 40-52), щелочная фосфатаза 80 МЕ / л (<160), АСТ 28 МЕ / л (диапазон 5-55) и гаммаглутамил трансфераза (ГГТ) 27 МЕ / л (диапазон 0-55). электролитные исследования были в пределах нормы, концентрация креатинина в сыворотке была 177 мкмоль / л (диапазон 55-120 мкмоль / л) и креатинина клиренс составил 42 мл / мин, протеинурии не было. Во время пребывания пациента в стационаре отмечались повторяющиеся приступы печеночной энцефалопатии, часто сопровождающиеся эпизодами спонтанного бактериального перитонита. Пациенту была выполнена ортотопическая трансплантация 16 января 1988 года. Во время трансплантации он был в печеночной коме IV степени.
У этого пациента были гистологические доказательства узловой регенеративной гиперплазии, но клинические находки относились к декомпенсированному циррозу печени.
Этот отчет показывает, что узловая регенеративная гиперплазия (NRH)может быть представлена конечной стадией печеночной недостаточности и это является напоминанием о том, что клинический диагноз без гистологического исследования может быть ошибочным.
Также, хочу еще раз обратить внимание на "несоответствие" изменений лабораторных показателей, в частности т.н. "печеночной панели" и тяжелых, можно сказать фатальных, клинических проявлений печеночной недостаточности возможных при NRH, которая в настоящее время признается наиболее частой причиной NCPH.
 Nodular_regenerative_hyperplasia_mimicking_0D_cirrhosis_of_the_liver__ENG_.pdf ( 1,07 мегабайт )
: 898
Nodular_regenerative_hyperplasia_mimicking_0D_cirrhosis_of_the_liver__ENG_.pdf ( 1,07 мегабайт )
: 898Автор: Stesha 15.02.2021 - 13:54
Добрый день, Ocean_ovna!
Спасибо Вам за очень важную и редкую информацию, представленную в этой теме! Немного странно, правда, что здесь нет активного отклика специалистов и обсуждения.
Cкажите, пожалуйста, кроме таких препаратов (преимущественно органических) как Гептрал, Гепа-Мерц, Дюфалак и Мелатонин можно ли применять гирудотерапию?
Ваш текcт:
"PS. Скорее всего, на ранних стадиях, если гипотетически предположить, что удалось поставить правильный диагноз, уместно назначение антикоагулянтов, так как ведущая роль в патогенезе этих состояний отводится облитерирующей венопатии терминальных вен. Также целесообразно с патогенетической точки зрения применение неселективных бета-блокаторов (карведилол, пропранолол)с целью уменьшения портального давления. Думаю, это не только приводит к профилактике кровотечений из варикозно-расширенных вен пищевода (о чем все пишут), но и в целом улучшает портальную гемодинамику, вероятно уменьшая скорость прогрессирования заболевания, хотя и возможность гепатотоксичности препаратов сбрасывать со счетов нельзя, поэтому необходим периодический контроль хотя-бы маркеров цитолиза (АЛТ/АСТ)"
Автор: Ocean_ovna 15.02.2021 - 14:26
Спасибо Вам за очень важную и редкую информацию, представленную в этой теме! Немного странно, правда, что здесь нет активного отклика специалистов и обсуждения.
Добрый день, Stesha! Спасибо за вопрос!
Для меня это тоже странно) или врачам это не интересно. Все равно это удивляет.
Ваш текcт:
"PS. Скорее всего, на ранних стадиях, если гипотетически предположить, что удалось поставить правильный диагноз, уместно назначение антикоагулянтов, так как ведущая роль в патогенезе этих состояний отводится облитерирующей венопатии терминальных вен. Также целесообразно с патогенетической точки зрения применение неселективных бета-блокаторов (карведилол, пропранолол)с целью уменьшения портального давления. Думаю, это не только приводит к профилактике кровотечений из варикозно-расширенных вен пищевода (о чем все пишут), но и в целом улучшает портальную гемодинамику, вероятно уменьшая скорость прогрессирования заболевания, хотя и возможность гепатотоксичности препаратов сбрасывать со счетов нельзя, поэтому необходим периодический контроль хотя-бы маркеров цитолиза (АЛТ/АСТ)"
Я не готов комментировать нетрадиционные методы лечения, но вероятно в вашем вопросе есть определенный смысл. Одно условие для использования как антикоагулянтов, так и герудотерапии достаточно сложно выполнимо - постановка правильного диагноза на ранних стадиях заболевания. Биохимия и печеночная панель практически малоинформативны. Биопсия печени при таких условиях соответственно маловероятна. Должна быть "настороженность" врачей в отношении этой патологии. Но в целом, под контролем коагулограммы, возможно и в гирудотерапии есть смысл.
Автор: Stesha 15.02.2021 - 15:30
Для меня это тоже странно) или врачам это не интересно. Все равно это удивляет.
Я не готов комментировать нетрадиционные методы лечения, но вероятно в вашем вопросе есть определенный смысл. Одно условие для использования как антикоагулянтов, так и герудотерапии достаточно сложно выполнимо - постановка правильного диагноза на ранних стадиях заболевания. Биохимия и печеночная панель практически малоинформативны. Биопсия печени при таких условиях соответственно маловероятна. Должна быть "настороженность" врачей в отношении этой патологии. Но в целом, под контролем коагулограммы, возможно и в гирудотерапии есть смысл.
Скорее всего, такое понятие как "настороженность" врачей осталось в СССР, а сейчас действуют протоколы и алгоритмы, прописанные свыше. Только, если врач заинтересован в поиске способов диагностики и лечения для себя или близких, может быть проделана работа, подобная Вашей.
У меня как раз такой случай, когда биохимия и УЗИ (местечково-допотопное) в норме, но есть многое из того, что Вы описали и что РЕАЛЬНО мешает жить: вздутия-запоры, ангиоэктазии на колоно, нарушения венозного оттока, полное отсутствие сил, боли в спине, нарушение зрения, печеночные ладони, белые ногти и многое другое. Но, так как АЛТ/АСТ норма, то все вышеперечисленное - это "психосоматика", а посему, игнорируется. Назначается лечение, в лучшем случае, поддерживающе-симтоматическое, в худшем с массой побочек. Вот, ищу способы поддержать себя альтернативой таблеткам. Хотя, понимаю, что побочки и противопоказания есть и у нетрадиционной медицины.
Автор: Ocean_ovna 15.02.2021 - 17:26
У меня как раз такой случай, когда биохимия и УЗИ (местечково-допотопное) в норме, но есть многое из того, что Вы описали и что РЕАЛЬНО мешает жить: вздутия-запоры, ангиоэктазии на колоно, нарушения венозного оттока, полное отсутствие сил, боли в спине, нарушение зрения, печеночные ладони, белые ногти и многое другое. Но, так как АЛТ/АСТ норма, то все вышеперечисленное - это "психосоматика", а посему, игнорируется. Назначается лечение, в лучшем случае, поддерживающе-симтоматическое, в худшем с массой побочек. Вот, ищу способы поддержать себя альтернативой таблеткам. Хотя, понимаю, что побочки и противопоказания есть и у нетрадиционной медицины.
Ну, белые ногти к психосоматике как-то тяжело прилепить, все же это ближе к обьективным проявлениям, хотя зачастую игнорируемым. А что заставляет подозревать печеночную патологию, были гепатотоксические факторы в анамнезе?
Автор: Stesha 16.02.2021 - 11:03
А что относится к гепатотоксичным факторам? Желтухи не было. Был очень сильный зуд тела, который прошел после приема гепабене и желчегонного сбора. Напрягают ангиоэктазии в кишечнике. Если они есть, то наверное есть портальная гипертензия, а ее причина - патология печени? Возможны кишечные кровотечения?
Автор: Ocean_ovna 16.02.2021 - 14:42
К гепатотоксичным факторам я бы прежде всего отнес алкоголь и систематический прием медикаментов.
Насколько понял, других данных - расширение воротной вены по результатам УЗИ и/или КТ/МРТ, вариксы в пищеводе по результатам ЭФГДС, увеличения селезенки - в пользу вероятной портальной гипертензии нет?
Могут быть и внепеченочные причины портальной гипертензии. Кровотечения, как правило, характерны для варикозно расширенных вен пищевода. По крайней мере, они считаются наиболее опасными для жизни. Геморроидальные кровотечения обычно менее обильны.
Автор: ama7ed 16.02.2021 - 15:38
Как я понял, при кровотечениях пищевода главная опасность состоит в том, что сгустки крови забивают дыхательные пути
Автор: Ocean_ovna 16.02.2021 - 15:57
Нет), Основная опасность кровотечения в самом кровотечении, т.е. потере обьема циркулирующей крови со всеми вытекающими последствиями - шок и т.д.
Автор: ama7ed 16.02.2021 - 16:45
Просто когда-то давным давно один патологоанатом выкладывал пост на эту тему, там с фотографиями вскрытия прямо было, сгустки крови застыли и закупорили бронхи. Ну, может быть, это была еще одна из причин.
Ну, и как я понял, если удастся выжить, то в ближайшее время все это будет повторяться снова и снова.
Автор: Stesha 18.02.2021 - 16:18
Добрый день, Ocean_ovna!
Да, алкогольный фактор существенный раньше был ))).
По ЭФГДС все в норме. А расширение воротной вены не ясно - есть или нет. По УЗИ лет десять назад был жировой гепатоз, а сейчас, якобы, все норме, кроме утолщенных стенок ЖП. Но, я не доверяю местному уровню сделанных УЗИ, надо сделать где-то на хорошем оборудования и у спеца. Не знаете, где в Москве можно сделать так, чтоб наверняка? Может быть лучше сделать МРТ брюшной полости? Оно более информативно чем УЗИ? Эластометрия - это как дополнение к УЗИ или МРТ, или ее вообще лучше не делать? Читала много отзывов, где ее результаты не сходятся в разных клиниках и только запутывают.
А какие еще бывают причины портальной гипертензии? Из жалоб еще сухость, покраснение и зуд кожи похожие по описанию на нейродермит. Повышенное давление 150-160 на 85-95, ниже 140 на 80 без таблеток не бывает. Самое тяжкое в состоянии это постоянное ощущение отечности и распирание в голове особенно к вечеру. На затылке лежать очень некомфортно. Засыпаю с трудом, только с помощью роликов с гипнозом и медитациями. Утром красные отекшие глаза и опухшее лицо, отек с лица к обеду немного спадает. Иногда пью валокардин перед сном, но тогда утром тяжело вставать. Вчера перед сном выпила супрастин и - ЧУДО! утром встала в значительно лучшем состоянии, чем всегда.
Автор: Ocean_ovna 18.02.2021 - 18:30
Да, алкогольный фактор существенный раньше был ))).
Добрый день, Stesha!
А как долго был и какой сейчас возраст?
Что касается причинной роли алкоголя, то существует стереотип, который закрепился в уме врачей в своеобразную догму о том, что алкогольная болезнь печени (АБП)существует сугубо в рамках т.н. континуума АБП, о котором я уже упоминал в этой теме, хотя хорошо известно что один и тот же патогенный фактор может приводить к разным болезням. Вероятные причины, по которым обсуждаемые патологии не рассматриваются практическими врачами возможными при АБП я тоже изложил - основные это плохое их знание и малоинформативность при них изменений биохимических показателей и аппаратных методов исследования (УЗИ/КТ/МРТ/Фиброскан)вплоть до конечных стадий заболевания печени - это очень хорошо иллюстрирует случай пациента, описанный в сообщении #14 этой темы. Он хорошо демонстрирует, что принцип - "чем выше/ниже биохимический показатель - тем хуже" - для заболеваний печени работает далеко не во всех случаях.
А какие еще бывают причины портальной гипертензии? Из жалоб еще сухость, покраснение и зуд кожи похожие по описанию на нейродермит. Повышенное давление 150-160 на 85-95, ниже 140 на 80 без таблеток не бывает. Самое тяжкое в состоянии это постоянное ощущение отечности и распирание в голове особенно к вечеру. На затылке лежать очень некомфортно. Засыпаю с трудом, только с помощью роликов с гипнозом и медитациями. Утром красные отекшие глаза и опухшее лицо, отек с лица к обеду немного спадает. Иногда пью валокардин перед сном, но тогда утром тяжело вставать. Вчера перед сном выпила супрастин и - ЧУДО! утром встала в значительно лучшем состоянии, чем всегда.
Внепеченочных причин портальной гипертензии достаточно много, например синдром Бадда-Киари или тромбоз печеночной вены. Я не ставил задачу описать их в этой теме, т.к. обратиться к локальным патологиям заставил личный опыт постановки правильного диагноза, как вы правильно заметили.
Что касается обследования в Москве, вероятно рекомендовал бы обратиться к профессору Буеверову Алексею Олеговичу. Мне кажется он грамотный и вдумчивый гастроэнтеролог-гепатолог и мог бы помочь вам своими рекомендациями в составлении индивидуальной программы обследования.
Автор: Stesha 19.02.2021 - 12:34
Ocean_ovna, благодарю Вас за отклик и информацию!
Автор: Doc Martin 13.03.2021 - 18:20
Интересная обобщающая статья по узловой регенеративной гиперплазии печени, опубликованная коллективом польских авторов во Всемирном гастроэнтералогическом журнале в 2011 году. Перевод статьи на русский в прикрепленном файле Ru (в нем нет таблиц и списка рекомендованной литературы из оригинала статьи.
 NRH_Evolving_concepts_Ru.pdf ( 460,8 килобайт )
: 624
NRH_Evolving_concepts_Ru.pdf ( 460,8 килобайт )
: 624 NRH_Evolving_concepts_Eng.pdf ( 775,19 килобайт )
: 947
NRH_Evolving_concepts_Eng.pdf ( 775,19 килобайт )
: 947Автор: ama7ed 14.03.2021 - 11:02
Отличная статья, написанная аж 10 лет назад.
Интересно, такое малое количество больных с НРГ обусловлено лишь тем, что только они обратились к врачу, для установки диагноза? А сколько ещё людей даже не подозревают об этом?
Автор: Ocean_ovna 15.03.2021 - 22:56
Интересно, такое малое количество больных с НРГ обусловлено лишь тем, что только они обратились к врачу, для установки диагноза? А сколько ещё людей даже не подозревают об этом?
Для ответа на этот вопрос, обратил бы внимание на цитату из статьи - "Следует подозревать диагноз НРГ у всех пациентов с клиническими симптомами портальной гипертензии (спленомегалия, вариксы пищевода, асцит), но с нормальными
трансаминазами и отсутствием проявлений цирроза печени (гинекомастия, ладонная
эритема, паутинные невусы)".
Добавил бы, что эти три признака портальной гипертензии могут иметь место в любых сочетаниях или изолированно, и трактовка увеличения селезенки (спленомегалии)на УЗИ чуть ли как нормы вызывает большие вопросы к профессиональной компетентности доктора.
Автор: ama7ed 16.03.2021 - 11:52
трансаминазами и отсутствием проявлений цирроза печени (гинекомастия, ладонная
эритема, паутинные невусы)".
Добавил бы, что эти три признака портальной гипертензии могут иметь место в любых сочетаниях или изолированно, и трактовка увеличения селезенки (спленомегалии)на УЗИ чуть ли как нормы вызывает большие вопросы к профессиональной компетентности доктора.
У меня есть один паучий невус, слева на груди, небольшой, правда.
А варикоцеле может указывать на НЦПГ? В литературе описано как застой крови в венах почки либо ее опухоль, по идее, НЦПГ тоже быть основным фактором?
Автор: Ocean_ovna 16.03.2021 - 13:36
Нет, не может. Кровоснабжение яичка к портальной системе никакого отношения не имеет, от слова "совсем".
Автор: Stesha 22.03.2021 - 16:11
Причиной варикоцеле также может быть синдром аортально-мезентериального пинцета.
Автор: ama7ed 24.03.2021 - 16:53
Интересно, НЦПГ и НРГ всегда сосуществуют вместе или были случаи, когда люди, имея НЦПГ при биопсии ничего не находили?
Автор: Ocean_ovna 24.03.2021 - 18:41
Вероятно все от подготовки и настороженности гепатопатолога зависит. При (не)желании или незнании можно и "ничего не найти".
Насчет сосуществования - может быть на самых ранних стадиях заболевания НРГ портальная гипертензия еще не проявляется клинически, но скорее всего процессы непосредственно связаны между собой. По сути, абревиатура НЦПГ просто констатирует наличие портальной гипертензии при отсутствии цирроза печени.
Автор: ama7ed 24.03.2021 - 21:48
Насчет сосуществования - может быть на самых ранних стадиях заболевания НРГ портальная гипертензия еще не проявляется клинически, но скорее всего процессы непосредственно связаны между собой. По сути, абревиатура НЦПГ просто констатирует наличие портальной гипертензии при отсутствии цирроза печени.
То есть, НЦПГ это последствия НРГ? Всегда думал, что наоборот.
Автор: Ocean_ovna 24.03.2021 - 23:57
Вряд ли в интактной печени "вдруг" появится внутрипеченочная портальная гипертензия. Однозначно, должен быть "материальный субстрат" к ней приводящий. уж какого уровня (изменения ультраструктуры гепатоцитов, дезорганизация паренхимы, а может быть их сочетание ) - это уже другой вопрос. По крайней мере, этому учит попираемый ныне всеми, кому ни попадя, диалектический материализм. Если это отрицать, тогда придется признавать эффективность лечения у шаманов и заклинаний апологетов течения религии вуду.
Автор: ama7ed 29.03.2021 - 10:00
По фиброзу еще интересное наблюдение: как мы знаем, у больных гепатитом известны случаи возврата стадии с F4 до F2 и даже F1. Но также есть известный факт, что при завышенных показателях АСТ/АЛТ при эластометрии жесткость всегда имеет высокие значения даже при нормальной печени.
Так вот вопрос: может ли быть такое, что на самом деле F4 на эластометрии имеет такие высокие показатели именно из-за АЛТ/АСТ, и когда больной со временем излечивает гепатит и возвращает нормальные показатели биохимии, то и эластометрия определяет меньшую стадию фиброза?
Автор: Ocean_ovna 29.03.2021 - 19:30
Так вот вопрос: может ли быть такое, что на самом деле F4 на эластометрии имеет такие высокие показатели именно из-за АЛТ/АСТ, и когда больной со временем излечивает гепатит и возвращает нормальные показатели биохимии, то и эластометрия определяет меньшую стадию фиброза?
Абсолютно верно!
Автор: Dmitry 10.04.2021 - 13:36
Здравствуйте, Ocean_ovna! Попал на Эластографию печени, и при моем, в принципе, более менее состоянии, я получил плохой результат... Прилагаю:
В Жильберщиках рассказывал о печеночных показателях и тромбофилии. И есть вопрос, где можно найти хорошего гепатолога в России, а то беда. Причин явных в возникновении такого фиброза не вижу. Результаты на гепатиты С и В отрицательные, правда еще не сдавал коагулограмму и альбумин...
Автор: Ocean_ovna 10.04.2021 - 19:02
В Жильберщиках рассказывал о печеночных показателях и тромбофилии. И есть вопрос, где можно найти хорошего гепатолога в России, а то беда. Причин явных в возникновении такого фиброза не вижу. Результаты на гепатиты С и В отрицательные, правда еще не сдавал коагулограмму и альбумин...
Добрый день, Dmitry!
По большому счету нужно исключать все, наиболее частые причины фиброзирования печени - кроме вирусных гепатитов это болезнь Вильсона-Коновалова, дефицит альфа1антитрипсина, гемохроматоз, первичный биллиарный цирроз и аутоиммунный гепатит - это как минимум. С селезенкой, я так понимаю все в порядке, соответственно данных за НЦПГ практически нет (по крайней мере пока нет). А как у Вас с уровнем тромбоцитов?
По поводу гепатолога в Пензе никакой информации дать не могу.
Возможно, для уточнения степени фиброза потребуеися биопсия печени, если по лабораторным данным причину установить будет невозможно.
По большому счету F2 это почти здоровая печень), по мнению большинства гепатологов, но причину в любом случае установить очень желательно, так как это может быть ключевым моментом если не для уменьшения фиброза, то хотя бы к замедлению его прогрессирования.
Если, все же, дело дойдет до биопсии печени, то неплохо было-бы получить т.н. "второе мнение" у патолога, специализирующегося по печени, возможно заграницей. Лично у меня вызывает доверие, основанное на изучении многих медицинских публикаций, отделение патологии университетской клиники г. Левен (Бельгия).
Автор: Dmitry 10.04.2021 - 20:19
По большому счету нужно исключать все, наиболее частые причины фиброзирования печени - кроме вирусных гепатитов это болезнь Вильсона-Коновалова, дефицит альфа1антитрипсина, гемохроматоз, первичный биллиарный цирроз и аутоиммунный гепатит - это как минимум. С селезенкой, я так понимаю все в порядке, соответственно данных за НЦПГ практически нет (по крайней мере пока нет). А как у Вас с уровнем тромбоцитов?
По поводу гепатолога в Пензе никакой информации дать не могу.
Возможно, для уточнения степени фиброза потребуеися биопсия печени, если по лабораторным данным причину установить будет невозможно.
По большому счету F2 это почти здоровая печень), по мнению большинства гепатологов, но причину в любом случае установить очень желательно, так как это может быть ключевым моментом если не для уменьшения фиброза, то хотя бы к замедлению его прогрессирования.
Если, все же, дело дойдет до биопсии печени, то неплохо было-бы получить т.н. "второе мнение" у патолога, специализирующегося по печени, возможно заграницей. Лично у меня вызывает доверие, основанное на изучении многих медицинских публикаций, отделение патологии университетской клиники г. Левен (Бельгия).
Да я даже про Москву сразу подумал, чтобы обследоваться... Пойду сдаваться в областную больничку, посмотрим, что скажут. А иначе так и придется - сам себе назначай анализы и проверяй...
Анализ последний от 28 марта есть с тромбоцитами
Под вирусными гепатитами проверка на В и С - достаточно? или все надо проверять поголовно...
Автор: Dmitry 10.04.2021 - 20:33
Есть ли смысл сразу принимать Лактулозу (это я про аммиак) и цинк?
Автор: Ocean_ovna 10.04.2021 - 20:41
Анализ последний от 28 марта есть с тромбоцитами
Под вирусными гепатитами проверка на В и С - достаточно? или все надо проверять поголовно...
Обычно, кроме В и С исключают еще вирусный гепатит Е, цитомегаловирус и Эпштейн-Барр вирус (последние два ввиду возможности пожизненного носительства после первичного заражения (а по некоторым данным это до 90% популяции)кроме определения антител к ним, требуют определения методом ПЦР). Обследоваться на гепатит D (дельта) при отсутствии маркеров гепатита В практического смысла нет, поскольку для его размножения в клетках и развития инфекции необходимо, чтобы клетки были заражены вирусом гепатита В.
Насчет лактулозы - думаю в ее приеме больше позитива, чем ожидаемых побочных эффектов. Насчет цинка - убедительных данных по нему нет, хотя он входит в состав металлоферментов принимающих участие в расщеплении фиброзной ткани, соответственно его дефицит теоретически должен приводить к перераспределению динамического равновесия между деградацией и синтезом коллагена в пользу последнего, увеличивая степень фиброза. Сывороточная концентрация его не всегда отражает содержание в тканях, ну и возможное возникновение дефицита меди на фоне длительного приема цинка тоже нужно учитывать.
Автор: Dmitry 10.04.2021 - 21:29
Спасибо Вам большое! За ваши ответы, если бы не ваши сообщения, мне сложно было бы двигаться дальше, и вполне вероятно, я о своем здоровье ничего так и не узнал бы. Теперь хоть вектор есть, куда смотреть...
Автор: Dmitry 11.04.2021 - 08:51
Насчет лактулозы - думаю в ее приеме больше позитива, чем ожидаемых побочных эффектов. Насчет цинка - убедительных данных по нему нет, хотя он входит в состав металлоферментов принимающих участие в расщеплении фиброзной ткани, соответственно его дефицит теоретически должен приводить к перераспределению динамического равновесия между деградацией и синтезом коллагена в пользу последнего, увеличивая степень фиброза. Сывороточная концентрация его не всегда отражает содержание в тканях, ну и возможное возникновение дефицита меди на фоне длительного приема цинка тоже нужно учитывать.
А могут ли антикоагулянты наносить такой вред печени? Может вопрос риторический... Я все переживаю по поводу их приёма... Мне остался ещё месяц принимать полную дозу, потом надо сдать тест на тромбодинамику, коагулограмму я сдам завтра.
Автор: Dmitry 11.04.2021 - 09:25
Хотя есть интересные статьи о том, что есть перспектива как раз принимать антикоагулянты при циррозах
https://www.actabiomedica.ru/jour/article/view/2041/1858
Автор: Ocean_ovna 11.04.2021 - 21:17
https://www.actabiomedica.ru/jour/article/view/2041/1858
Спасибо. Интересная статья.
Применительно к вашей ситуации приведу из нее цитату "Установлено, что активация коагуляционного каскада не только повышает риск тромбозов, но и играет большую роль в повреждении печени, способствуя прогрессированию фиброза", т.е. тромбофилическое состояние вполне может быть обьяснением не только заболеваний печени связанных с НЦПГ но и фиброза печени. Жаль, что до терапии антикоагулянтами не назначили полного обследования коагуляционного статуса (коагулограмма, протеин С и S, антитромбин III, тест генерации тромбина), а не только генетические тесты.
Автор: Stesha 14.04.2021 - 23:28
Добрый день! Что скажете насчет такого варианта лечения?
Для специалистов здравоохранения!
Консервативное лечение гепатита C помощью триады антиоксидантов. Сочетанное использование альфа-липоевой (тиоктовой) кислоты, силимарина и селенметионина: три клинических случая
Статьи
Опубликовано в журнале:
Medizinishe Klinik ?? 1999; 94: Suppl III: 84-89
Burton M. Berkson
Integrative Medical Center of New Mexico and Applied Biology EPPWS Department, New Mexico State University, Las Cruces, New Mexico, USA
Автор: Stesha 14.04.2021 - 23:48
https://medi.ru/info/9063/
Автор: Ocean_ovna 15.04.2021 - 21:35
Спасибо. Интересная информация, хотя статья написана более 20 лет назад и схемы лечения, а соответственно и лекарственные средства для лечения хронического гепатита С значительно изменились с тех пор. Их эффективность увеличилась. Сложно сказать, почему при таком позитивном эффекте от предложенной терапии, она все же за прошедшие годы не получила дальнейшего развития. Отчасти ответ на этот вопрос дают сами авторы статьи мотивируя эту ситуацию тем, что "В Америке интерес к применению АЛК при отравлениях грибами и других заболеваниях печени был утерян в основном из-за того, что операцию по трансплантации печени стали считать "рутинной" в случаях тяжелых заболеваниях печени."
Возможно, что в качестве "терапии отчаяния" при отсутствии перспектив ТП она может быть и оправданной?
Автор: ama7ed 7.06.2021 - 11:29
Каждый раз, как перечитываю эту(и соседнюю) тему, то нахожу что-то новое, чего раньше не замечал.
Вот, например, открыл лекции доктора Буеверова А.О, очень интересные и грамотные вещи. Интересно, он принимает лично?
https://internist.ru/publications/detail/lechenie-pechenochnoy-encefalopatii-%E2%80%93-prakticheskie-rekomendacii/
Автор: Ocean_ovna 9.08.2021 - 08:55
Что можно добавить с момента размещения этой темы.
Анализ историй пациентов со всего мира зарегистрированных на британском форуме поддержки пациентов с заболеваниями печени https://healthunlocked.com/ (для доступа ко всем функциям форума необходима регистрация)показывает, что проблема диагностики НЦПГ/НРГ (по крайней мере прижизненной)существует во всем мире. Редкой ее назвать сложно. Ситуация приблизительно везде одинаковая. Получив отрицательные результаты биохимических тестов при отсутствии цирроза по результатам эластометрии или фиброскана (в данном случае их можно назвать ложными помощниками гепатолога и злейшими врагами пациента)от дальнейших диагностических поисков врачи пациентам, как правило, отказывают, даже при наличии у них клинических признаков энцефалопатии (которая как вероятная печеночная не рассматривается, а при относительно сохранных когнитивных функциях у пациентов вообще не диагностируется). За редким исключением случаев, когда у пациента, например, находят необьяснимо умеренно повышенные АЛТ/АСТ , могут назначить пункционную (не лапароскопическую) биопсию печени и при хорошем стечении обстоятельств (игла попала в нужное место, столбик ткани достаточного размера, гистологию оценивал хорошо подготовленный гепатопатолог) установить правильный диагноз.
О трансплантации печени этим пациентам речь не стоит вообще из-за ограничений МELD и связанной с этим предвзятостью отбора. Даже гипотетически набрав необходимые баллы и попав в лист ожидания трансплантации пациент с НЦПГ скорее всего будет пропускать вперед всех пациентов с циррозом до развития фатального исхода заболевания (печеночной комы). Единицы из пациентов с НЦПГ/НРГ/НЦПФ подвергаются трансплантации в отдельных трансплантационных центрах западных стран, врачи которых достаточно информированны о проблеме диагностики и клиники НЦПГ и руководствуются в своей деятельности рекомендациями EASL по трансплантации печени для пациентов с ограничением MELD.
Ждать изменений в диагностических подходах можно многие годы, если не десятилетия, а пациентам нужна адекватная помошь именно сейчас.
Что же делать в такой ситуации?
Вероятно нужен какой-то алгоритм для пациента, который бы помог ему максимально, на сколько это возможно, не оказаться без адекватной медицинской помощи и не пойти по ложному пути диагностического поиска.
Если подозревается печеночная энцефалопатия, нужно очень быстро начинать эмпирическую терапию. На сегодняшний день для эмпирической терапии печеночной энцефалопатии существует три препарата, которые используются либо последовательно, либо одновременно. Это Дюфалак/Лактулоза ("Lactulose"), Альфа-нормикс/Рифаксимин ("Rifaximin") и Гепа-мерц/ L-орнитин-L-аспартат.
Прежде всего, при наличии у пациента с подозрением на хроническое заболевание печени в отсутствии цирроза печени (может помочь в выявлении наличие у пациента "гепатотоксичного" анамнеза (алкоголь, лекарства, БАДы и травяные сборы, высокие дозы витаминов особенно жирорастворимых, препараты для похудения, гормональные контрацептивы и др. "Среди лекарственных препаратов, которые вызывают развитие фиброза печени с портальной гипертензией важное место занимают метотрексат, триоксид мышьяка и витамин А, а также другие гепатотоксические препараты - парацетамол, вальпроат натрия, амиодарон, изониазид и галотан, сульфаниламиды, азатиоприн, половые гормоны"
Медицинские Диссертации http://medical-diss.com/medicina/fibrozy-pecheni-patogenez-klinika-diagnostika#ixzz78TqZj4MA
и наличие "печеночных знаков" хронической печеночной патологии - печеночные ладони или пальмарная эритема, стойкий светлый стул, телеангиоэктазии на коже, ногти Терри, гинекомастия у мужчин, геморрой как весьма вероятное проявление портальной гипертензии) имеющихся клинических проявлений энцефалопатии неясной этиологии в виде слабости, повышенной немотивированной утомляемости, инверсии сна (спит днем, бессонница ночью), бессонницы, появлении нарушения координации и атаксии, несинхронного бокового тремора пальцев и языка, мозгового "тумана", преходящего или постоянного тиннитуса, сладкого/сладко-фекального/рыбного ("fetor hepaticus")запаха изо рта особенно по утрам, мышечных подергиваний в разных участках тела (желательно лабораторно исключить возможный дефицит В12 по уровню В12 в крови и гомоцистеина, как маркера функционального дефицита В12)- нужно подозревать печеночную энцефалопатию (ПЭ) и попробовать пробную терапию лактулозой по 25 -30-40мл 3 раза в день (доза подбирается индивидуально до мягкого стула не менее двух и не более трех раз в сутки) с одновременным ограничением белка в питании до 1.3-1.5 г на кг массы тела и уменьшением квоты животного белка. У пациентов с нарушением нутритивного статуса и потерей массы тела и мышечной массы необходима нутритивная поддержка и общая калорийность суточного рациона около 2500ккал. Пищу нужно принимать дробно, на протяжение дня небольшими порциями с обязательным поздним приемом пищи.
Альтернативным или дополнительным препаратом для лечения ПЭ с подтвержденной эффективностью является невсасывающийся антибиотик рифаксимин (альфа-нормикс, ксифаксан, Альфаксим (Россия)), который может назначаться длительным курсом по 550мг (ксифаксан)2 раза в сутки или по 400мг (альфа-нормикс по 2 таб. 200мг)3 раза в сутки.
Третьим препаратом с относительно подтвержденной эффективностью считается L -орнитина L -аспартат (Гепа-Мерц), который назначается в виде курсового (по 2 месяца с 2-х месячным перерывом) или постоянного приема по 1-2 саше 3 раза в день.
При неэффективности пробной терапии ПЭ в течение 2-х месяцев необходимо уточнить диагноз.
Наиболее достоверным аппаратным методом диагностики при подозрении на НЦПГ в продвинутой стадии болезни считаю доплер сосудов брюшной полости с измерением скорости кровотока в портальной системе (верхняя брыжеечная, селезеночная и воротная вены). В такой ситуации, кровоток в этих сосудах будет ускорятся из-за развития коллатерального кровообращения в мелких сосудах не визуализирующихся на УЗИ (также УЗИ не доступна визуализация вен пищевода и околоректальных анастомозов)или в результате шунтирования через парапортальные шунтирующие сосуды (порто-кавальные анастомозы) в самой печени (ускоряется кровоток в воротной вене). Размер самой воротной вены и селезенки может оставаться в норме из-за шунтирования и постепенного медленного развития патологического процесса и как показано в ряде зарубежных исследований не является достоверным диагностическим критерием позволяющим исключить портальную гипертензию.
Автор: Ocean_ovna 22.09.2021 - 21:18
Ещё две интересные работы в которых указывается о целесообразности применения LoLa (Гепа-Мерц) при использовании ВСАА (аминокислоты с разветвленной сетью) в лечении саркопении и печеночной энцефалопатии (ПЭ) так как орнитин может ослабить потенциально опасное воздействие ВСАА на катаплероз.
Обоснование рекомендации по применению аминокислот с разветвленной цепью (BCAA; валин, лейцин и изолейцин) для лечения печеночной недостаточности основано на их уникальных фармакологических свойствах, стимулирующем действии на детоксикацию аммиака до глутамина и пониженных концентрациях при печеночной недостаточности. Многочисленные исследования показали, что основной причиной дефицита BCAA при печеночной недостаточности является их потребление в скелетных мышцах для синтеза глутамата, который действует как субстрат для детоксикации аммиака до глутамина, и что введение BCAA пациентам с печеночной недостаточностью может вызвать ряд положительных эффектов, которые могут быть более выраженными у пациентов с выраженным снижением уровня BCAA. С другой стороны, из-за стимулирующего действия BCAA на синтез глутамина, добавление BCAA может привести к усилению выработки аммиака в результате распада глутамина в кишечнике и почках и, таким образом, оказать негативное воздействие на развитие печеночной энцефалопатии. Следовательно, для повышения терапевтической эффективности BCAA у пациентов с повреждением печени необходимо предупреждать их негативное воздействия на выработку аммиака, которое незначительно у здоровых людей и / или пациентов с другими заболеваниями. При лечении печеночной энцефалопатии предлагается одновременное введение BCAA (для коррекции аминокислотного дисбаланса и ускорения детоксикации аммиака до глутамина) с L-орнитином L-аспартатом (LOLA), α-кетоглутаратом (для ингибирования распада глутамина на аммиак в энтероцитах) и / или фенилбутирата (для увеличения выведения глутамина почками).
α-Кетоглутарат - один из важнейших переносчиков аммиака в метаболических путях. Аминогруппы от аминокислот прикрепляются к α-кетоглутарату в реакции трансаминирования и переносятся в печень, попадая в цикл мочевины или орнитиновый цикл. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4703346/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7423914/
https://www.google.com/url?sa=t&source=web&rct=j&url=https://www.mediasphera.ru/issues/zhurnal-nevrologii-i-psikhiatrii-im-s-s-korsakova/2017/10/downloads/ru/1199772982017101144&ved=2ahUKEwiQ1PzvlJPzAhUymYsKHcUuDpIQFnoECAkQAQ&usg=AOvVaw3rmrNwQFDiKo-g6MqQIpms&cshid=1632334646446
Автор: Ocean_ovna 3.10.2021 - 20:26
Немного медицинской статистики об Узловой регенеративной гиперплазии печени (NRH).
Систематических исследований распространенности в популяции NRH не проводилось. Заболевание везде описывается словом "редкое", а большинство сообщений в медицинской литературе основано на описании единичных случаев. Единственное ретроспективное исследование с целью выяснения частоты его встречаемости в популяции было проведено по результатам исследования 2500 рандомных аутопсий, которое показало, что распространенность NRH составила 2,6%, Более того, в 10,2% этих случаев вскрытий были обнаружены различные степени узловых преобразований. Хочется сравнить с чем нибудь похожим... с циррозом например. В странах СНГ цирроз печени встречается у 1 % населения и к редким болезням его никто не относит. Значит редкость НРГ - медицинский миф? А редкие заболевания и редко диагностируемые заболевания это абсолютно не взаимозаменяемые понятия...
Распространенность узловой регенеративной гиперплазии (NRH) среди биоптатов печени составляет около 4% * . Среди тех, кто направлен по поводу необъяснимых нарушений ферментов печени, распространенность NRH выше и составляет 15% *.
* Barge S, Grando V, Nault JC, Broudin C, Beaugrand M, Ganne-Carriй N, Roulot D, Ziol M. Распространенность и клиническое значение узловой регенеративной гиперплазии в биоптатах печени. (2016) Liver international: официальный журнал Международной ассоциации по изучению печени.
https://radiopaedia.org/articles/nodular-regenerative-hyperplasia
Автор: ama7ed 4.10.2021 - 11:28
Систематических исследований распространенности в популяции NRH не проводилось. Заболевание везде описывается словом "редкое", а большинство сообщений в медицинской литературе основано на описании единичных случаев. Единственное ретроспективное исследование с целью выяснения частоты его встречаемости в популяции было проведено по результатам исследования 2500 рандомных аутопсий, которое показало, что распространенность NRH составила 2,6%, Более того, в 10,2% этих случаев вскрытий были обнаружены различные степени узловых преобразований. Хочется сравнить с чем нибудь похожим... с циррозом например. В странах СНГ цирроз печени встречается у 1 % населения и к редким болезням его никто не относит. Значит редкость НРГ - медицинский миф? А редкие заболевания и редко диагностируемые заболевания это абсолютно не взаимозаменяемые понятия...
Добрый день!
По недавним заметкам в интернете отечественных врачей-гепатологов и гастроэнтерологов и их перепискам по тому или иному пациенту, отмечался интересный факт : у многих пациентов, которым изначально ставили цирроз печени, отсутствовали как факт сами показатели цирроза, а значения выставлялись по причине печеночной энцефалопатии, повышения печеночных показателей в биохимии, на УЗИ отмечались увеличение и диффузность ткани, расширения воротной вен, а также увеличения селезенки, однако при эластометрии стадия фиброза у многих не заходила до F2. Также у пациентов присутствовали печеночные знаки.
После проведений дополнительных обследований, взятий биопсии и полной проверке анализов, у многих пациентов изначальный диагноз отменяли. Такая вот "редкая" болезнь...
Автор: Ocean_ovna 5.10.2021 - 22:21
Вот, просто любопытно, что же им выставляли по результатам биопсии?... Рад был бы ошибиться, но мне кажется, что ни один из отечественных гепатопатологов диагноз узловой регенеративной гиперплазии печени или гепато-портального склероза определить не способен... Будут максимум по Кноделю баллы подсчитывать...
Автор: ama7ed 6.10.2021 - 10:33
Да они Синдром Жильбера даже не выставляют, считают баллы, не обращая внимания на нормальные показатели биохимии и завышенный билирубин. Про НРГ еще не от одного врача не слышал, разве что только про очаговые узлы гиперплазии, к которым тоже привязываются основываясь исключительно на других сопутствующих данных, которых либо нет, либо не видно...
Автор: Ocean_ovna 19.11.2021 - 16:55
Новая информация по идиопатической нецирротической портальной гипертензии опубликована 3 ноября 2021 года.
Термин порто-синусоидальная сосудистая болезнь (porto-sinusoidal vascular disease, PSVD) был предложен Группой по изучению сосудистых заболеваний печени (VALDIG), которая недавно ввела термин "порто-синусоидальное сосудистое заболевание" (PSVD) для замены термина идиопатическая нецирротическая портальная гипертензия (INCPH) для описания пациентов с или без признаков портальной гипертензии и типичных гистологических поражений с вовлечением портальных венул и/или синусоидов в отсутствие цирроза печени. Этот недавно предложенный термин пытается преодолеть недостатки предыдущей терминологии, включая пациентов на более ранних стадиях без признаков портальной гипертензии. В соответствии с этим новым определением, клинический анамнез портальной гипертензии больше не требуется для диагностики PSVD, и достаточно обнаружения "специфических" гистологических признаков (включая облитерирующую портальную венопатию, узловую регенеративную гиперплазию (NRH) и неполный септальный цирроз (ISC) Согласно новому определению, наличие известных причин заболевания печени, а также тромбоза воротной вены не исключает PSVD. Следовательно, пациентов, у которых возможен диагноз PSVD, намного больше, чем пациентов, строго выполняющих диагностические критерии INCPH. В таких условиях клиническая задача гепатолога состоит в том, чтобы выявить пациентов с риском развития PSVD и назначить биопсию печени для подтверждения диагноза. Мы описываем некоторые возможные сценарии, при которых всегда следует подозревать PSVD, и предлагаем некоторые инструменты, полезные для диагностики PSVD.
"Диагноз PSVD, основанный на биопсии печени и общей уникальной номенклатуре, обеспечивает диагностические критерии, необходимые для будущих обобщающих исследований, чтобы изучить и определить характеристики и естественную историю этого нового объекта. Следует активно искать ПСВД как у пациентов с заболеваниями печени, так и у пациентов с внепеченочными ассоциированными состояниями. Как следствие, PSVD может быть менее редким, чем сообщается в настоящее время."
Полный текст оригинала статьи на английском доступен по ссылке
https://www.dovepress.com/identifying-patients-at-high-risk-of-developing-non-cirrhotic-portal-h-peer-reviewed-fulltext-article-HMER
Автор: Ocean_ovna 19.12.2021 - 18:22
Попалась, на мой взгляд, очень интересная статья в которой описывается исследование влияния добавок биотина (витамин В7) на морфологию печени и маркеры токсичности для печени. Самцов мышей кормили контрольной диетой или диетой с добавлением биотина в течение 8 недель. По сравнению с контрольными мышами, мыши, получавшие биотин, имели измененную портальную триаду с расширенными синусоидами, повышенной васкуляризацией и желчными протоками. Кроме того, наблюдалось увеличение доли гепатоцитов с увеличенными ядрами и двуядерных гепатоцитов, отражая, по всей видимости, усиление процесса регенерации гепатоцитов. Несмотря на морфологические изменения печени, различий в сывороточных показателях поражения печени, маркерах окислительного стресса и антиоксидантных ферментах не наблюдалось. Данные впервые демонстрируют, что добавка биотина приводит к морфологическим изменениям печени у нормальных мышей, и что эти изменения не коррелируют с биохимическими маркерами повреждения, маркерами окислительного стресса или антиоксидантных ферментных систем.
Выводы авторов статьи о таких изменениях морфологии печени весьма расплывчаты, но внимательный читатель этой темы заметит, что они "удивительным образом" совпадают с описанием морфологических изменений печени при нецирротической портальной гипертензии (НЦПГ), которую предлагается сейчас называть порто-синусоидальной сосудистой болезнью печени (PSVD).
Учитывая то, что развитие НЦПГ описано также при применении витамина А в высоких дозах, выскажу предположение, что многие ксенобиотики и токсиканты, лекарственные препараты, в том числе и синтетические витамины, вероятно, способны приводить к изменению морфологии печени по типу PSVD без изменения общепринятых сывороточных показателей повреждения печени и, вероятно, относительно длительное и необоснованное клинически и лабораторно применение синтетических витаминов, в отсутствии дефицитных по ним состояний, является опасным в плане развития PSVD, особенно при полном отсутствии биохимических маркеров такого повреждения для его возможного раннего выявления.
Эта информация представляет практический интерес, так как общепринятым считается относительная безопасность применения высоких доз витаминов группы В, избыток которых "просто" выводится из организма с мочой. Вероятно, все же, не так все "просто"...
Оригинал статьи на английском по ссылке https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5220432/
В настоящее время в клинической практике применяется классификация, предложенная в 1993 г. CIOMS (Council for International Organizations of Medical Sciences/Совет международных научных медицинских организаций), в основе которой лежит принцип оценки активности биохимических показателей сыворотки крови: аланиновой аминотрансферазы (АлАТ), щелочной фосфатазы (ЩФ) и билирубина. На основании полученных результатов выделяют три типа ЛПП: гепатоцеллюлярное, холестатическое и смешанное.
Гепатоцеллюлярное ЛПП характеризуется повышением активности АлАТ более чем в 2 раза в сравнении с верхней границей нормы (ВГН) или соотношением АлАТ/ЩФ >5. Данную форму ЛПП отличает более тяжелая степень поражения печени в сравнении с холестатической.
Сочетание гепатоцеллюлярного типа ЛПП с гипербилирубинемией характеризует тяжелое повреждение печени, сопряженное с высокой смертностью. Его частота составляет 0,7-1,3 на 100 тыс. пациентов, принимающих лекарственные препараты.
Холестатическое ЛПП - типично повышение активности ЩФ более 2 ВГН, или соотношение АлАТ/ЩФ <2.
Смешанный тип ЛПП - свойственно повышение активности АлАТ >2 ВГН и соотношение АлАТ/ЩФ >2, но <5.
У пациентов с холестатическим или смешанным типами ЛПП чаще встречается хроническое течение, с гепатоцеллюлярным типом острое течение.
Источник по ссылке https://cyberleninka.ru/article/n/gepatotoksichnost-antibakterialnyh-preparatov-v-terapevticheskoy-praktike
Автор: Ocean_ovna 5.01.2022 - 00:00
Заболевания связанные с узловой регенеративной гиперплазией печени (nodular regenerative hyperplasia, NRH) (T Roskams et al., Histopathology of portal hypertension: a practical guideline, 2003 )
Воспалительные заболевания печени
- Вирусные гепатиты
- Туберкулёз
- Саркоидоз
Болезни желчевыводящих путей
- Первичный билиарный цирроз
- Аутоиммунная холангиопатия
- Первичный склерозирующий холангит
Токсические повреждения печени
- Мышьяк
- Медь
- Винилхлорид
- Синдром токсического масла
- Иммуносупрессивные препараты
- Кортикостероиды
- Оральные контрацептивы
- Андрогенные анаболические стероиды
Системные заболевания
- Ревматоидный артрит с ревматоидным артерии том
- Синдром Фелти ( Ревматоидный артрит, лейкопения, спленомегалия)
- Системная красная волчанка
- Узелковый периартериит
- Аутоиммунный тиреоидит (болезнь Хашимото)
- Гипертиреоидизм
- Идеопатическая тромбоцитопеническая пурпура
- Моноклональные гаммапатии
- Диабет
- Амилоидоз
- Болезнь лёгких цепей
- Склеродермия
Другие состояния
- Наследственная геморрагическая телеангиэктазия
- Синдром Дауна
- Персистирующий венозный проток
- Гломерулонефрит
- Следствие почечного диализа или трансплантации почки при терминальной стадии почечной недостаточности
- В следствии трансплантации костного мозга
- Застойная сердечная недостаточность
- Подострый бактериальный эндокардит
- Недостаточность сердечных клапанов
- Первичная лёгочная гипертензия
Злокачественные опухоли
- Лимфома
- Болезнь Ходжкина
- Гистиоцитоз Х
- Другие злокачественные опухоли
Миелопролиферативные заболевания
- Истинная полицитемии
- Хроническая миелоидная лейкемия
- Миелоидная метаплазия
- Первичная тромбоцитемия
Хотя этот список причин НРГ обширен, он далеко не исчерпывает все возможности. В нем отсутствуют такие уже известные факторы, как целиакия и болезнь Крона. Последние данные показывают, что алкогольная болезнь печени (АБП) может приводить не только к циррозу, но и к узловой регенеративной гиперплазии и порто-синусоидальной васкулярной болезни (PSVD) печени. Это связано с флебосклерозом воротных венул и обструкцией синусоидов, что вызывает нецирротическую портальную гипертензию. Согласно современным рекомендациям, это необходимо учитывать при диагностике данных состояний, а также других известных причин, приводящих к цирротической трансформации печени.
Автор: Ocean_ovna 4.07.2022 - 01:48
Приведу ещё один случай, который иллюстрирует с какими трудностями приходится столкнуться пациенту с узловой регенеративной гиперплазией/нецирротической портальной гипертензией в постановке правильного диагноза.
Пациентка из Румынии, 42 года. В 14 лет перенесла гепатит неясной этиологии (со слов пациента), изредка курит, употребляла алкоголь в умеренных дозах. Около года назад отмечает начало манифестации симптомов в виде выраженной слабости, немотивированной потери веса, бессонницы, мышечных подергиваний и спазмов, постоянного сладко-солоноватого привкуса во рту, изменение вкуса табачного дыма, усиление пигментации кожи, выраженного снижение аппетита, периодической тошноты, "мозгового тумана", затуманенного зрения, головокружения. Пациентка заподозрила у себя заболевание печени, по поводу чего неоднократно консультировалась на родине и в Италии. Патология печени всеми консультантами отвергалась. Проведенные визуализирующие методы обследования (УЗИ, МРТ, КТ) не показали никаких отклонений, признаки портальной гипертензии не выявлены. Фибросканирование печени 5.6 кПа. Биохимия крови показала снижение уровня ферритина, повышенный уровень аммиака, креатинин и мочевина на верхней границе нормы, остальные показатели в том числе LFT в пределах референсного интервала, тромбоциты 440. На коже шеи, груди и живота визуализируются (по фото) единичные капельные ангиомы (симптом Тужилина), которые обычно связывают с хроническим панкреатитом (по моему мнению капельные ангиомы характерных локализаций могут быть аналогом паукообразных ангиом и тогда они связаны с портальной гипертензией).
В мае 2022 года в румынской клинике пациентке проведена пункционная биопсия печени.
"Пункция биопсии печени
Цилиндрический фрагмент биопсии ткани печени длиной 2 см, состоящий из ткани печени с сохраненной архитектурой, некоторые портальные тракты с легким фиброзом, без выраженных воспалительных элементов, с явлениями слабовыраженного холестаза в гепатоцитах вокруг центролобулярной вены. Отсутствие признаков стеатоза. Без гранулематозных элементов. Без опухолевых элементов.
Отрицательное окрашивание по Перлс.
ЗАКЛЮЧЕНИЕ: Фрагмент биоптата ткани печени без выраженных гистопатологических изменений.
Элементов злокачественности нет.
Соотнесите с клиническими аспектами и аспектами визуализации".
Стоит отметить, что гистологические образцы в этом случае окрашивались только гематоксилином-эозином и Perls (окраска на гемосидерин). Окраска на ретикулиновые волокна не проводилась из-за странного обоснования - "отсутствии такой необходимости".
Ввиду отсутствия проблем с печенью по биохимическим данным, визуализирующим методам обследования и результатам гистологии, состояние пациентки ошибочно интерпретировано как психосоматическое расстройство (это несмотря на высокий уровень аммиака (152!!! мкмоль/л)). Ей рекомендован прием амитриптилина и наблюдение у ....психиатра ![]() .
.
Пациентке дистанционно рекомендовано воздержаться от приема амитриптилина, начать лечение направленное на снижение уровня аммиака (лактулоза, рифаксимин, LoLa (Hepa-Merz)) и получить "второе мнение" по результатам проведенной гистологии в отделении патологии университетской клиники г. Левен (Бельгия). Для повторной оценки в отделение патологии пациенткой пересланы гистологические препараты и парафиновый блок (с целью возможности дополнительного окрашивания). В результате лечения пациентка отметила некоторое улучшение самочувствия. "Второе мнение" по гистологии печени интерпретировано как узловая регенеративная гиперплазия печени/нецирротическая портальная гипертензия и гепатопортальный склероз. В настоящее время пациентка собирается обратиться к специалисту специализирующемуся по сосудистым заболеваниям печени из группы экспертов VALDIG во Франции для выработки дальнейшей стратегии.
Скачать гистологический отчёт https://wdfiles.ru/f17c7b
Автор: NoWonder 13.08.2022 - 10:24
Жаль нет информации проверялся ли её биоптат на гепатиты. С учётом перенесённого когда-то гепатита неясной этиологии вполне вероятна ситуация, что в крови нет ничего, даже антител, а в биоптате будет РНК например гепатита Ц. Тогда скорее всего речь идёт о многолетнем латентном течении гепатита, который привёл к такому результату. Латентные гепатиты тоже ещё совсем новая страница в медицине, которая только начинает осознаваться.
Автор: Ocean_ovna 15.08.2022 - 16:20
Безусловно, эта информация интересна в академическом аспекте, но, к сожалению, на мой взгляд, она мало что внесёт в лечение пациента на этапе диагностики НЦПГ. Тем более, что сама эта диагностика вызывает практически непреодолимые трудности, связанные с плохой подготовкой как гепатологов, так и патоморфологов-гепатопатологов. Тем не менее, раз уж пациент дожил до биопсии, и она была проведена, то должны быть использованы все доступные методы для правильной ее интерпретации, в том числе и с учётом анамнестических данных у конкретного пациента. К сожалению, сейчас в подавляющем числе случаев, насколько я могу судить, процесс окраски гистопрепаратов происходит стандартно "по умолчанию", максимум 2-3 методами, доступными в конкретном патоморфологическом отделении.
Автор: Стахий 11.09.2022 - 22:05
Хотелось бы спросить,на моем фото это тоже ангиомы?
Автор: Ocean_ovna 12.09.2022 - 12:48
Да, это ангиомы.
Автор: Стахий 13.09.2022 - 18:00
Как я понимаю,судя по разным косвенным признакам, все- таки у меня нецирротическая портальная гипертензия?
Автор: Ocean_ovna 13.09.2022 - 20:36
Скажем так, вероятность достаточно высока. Я посмотрел Ваши первые сообщения, в одном из которых Вы писали - "Насчет портальной гипертензии начали говорить после КТ, там в результатах говорилось о признаках ПГ,а потом сделали УЗДГ и как бы не подтвердили." Я уже комментировал подобную ситуацию у другого пациента - нельзя исключать данные полученные более точным методом исследования с помощью менее точного метода - это нонсенс. Весьма вероятно, что рост числа ангиом в последнее время (после ОИМ) связан с усилением синусоидальной обструкции и соответственно ПГ на фоне проводимого лечения. К сожалению, как я уже писал в этой ветке, не все аспекты гепатотоксичности лежат в плоскости изменения уровня трансаминаз. Возможны также морфологические изменения печени по типу синусоидальной обструкции (PSVD) без изменения биохимических показателей и это вовсе не говорит о "лёгкости" процесса. В Вашем случае, с одной стороны, отмена проводимого противорецидивного лечения ССЗ чревата ухудшением клинической ситуации по кардиологии, с другой стороны - продолжение терапии гипотетически может ухудшать ситуацию со стороны печени. Непростая клиническая ситуация... В такой ситуации, на мой взгляд, необходимо уменьшить лекарственную нагрузку до минимально допустимой, за счёт оптимизации применяемых доз лекарственных препаратов, под контролем биохимических показателей (холестерин и его фракции, коагулограмма, печёночная панель). Коррекция дефицита витамина Д, в случае необходимости под лабораторным контролем до достижения оптимального уровня 40 - 60 нг/мл. . Для количественной оценки витамина D в крови рекомендуется определять содержание метаболита 25 (ОН) D, а не активной формы 1,25 (ОН) 2 D, так как при дефиците витамина D содержание 1,25 (ОН) 2 D может быть как пониженным, так и нормальным или даже повышенным. Также имеются данные о том, что эффективность комбинации малых доз статинов и урсодезоксихолевой кислоты выше, чем использование удвоенной дозы статинов. То есть, другими словами, сочетание статина с урсодезоксихолевой кислотой в дозе 10-15 мг/кг в сутки позволяет как минимум вдвое уменьшить дозу статина. Урсодезоксихолевая кислота уменьшает воспаление в печени и улучшает дисфункцию эндотелия синусоидов. По безопасности крестора/розувастатина (именно для печени) ничего сказать не могу. Работ по этому препарату не очень много, так как он относительно новый. В основном большинство работ по безопасности статинов при печеночной патологии проводилось по симвастатину и некоторые исследования по аторвастатину. Несмотря на гепатотоксичность для этих препаратов описывают так называемые плейотропные эффекты, т.е. позитивное влияние не только на липидный профиль. В экспериментальных моделях в подавляющем числе наблюдений плейотропные эффекты статинов были получены при использовании таких низких доз статинов, которые не могут повлиять на уровни липидов.Так статины помимо гиполипидемических свойств способны улучшать дисфункцию эпителия синусоидов печени. Это связано с повышением биодоступности оксида азота NO в цирротически измененной печени, что приводит к уменьшению периферического сосудистого сопротивления ПСС в печени и уменьшению портального давления без негативного влияния на системную гемодинамику. Кроме того, не исключается, что положительное действие статинов на ПГ обусловлено ослаблением резистентности естественных портосистемных шунтов. Вероятно, в комплекс лечения целесообразно включить терапию направленную на снижение уровня аммиака, неоднократно описанную мной (лактулоза (Дюфалак), Гепа-Мерц (Орнитин-Канон(Россия)), рифаксимин (Альфа-нормикс/Аальфаксим (Россия)).
Автор: Стахий 14.09.2022 - 21:21
Спасибо за подробный ответ! НО всё таки я никак не могу понять,если я правильно понимаю,портальная гипертензия происходит когда печеночные клетки гибнут ,и ухудшается оток крови.А у нас(Жильберщиков) печеночные ферменты все в норме ,клетки не гибнут.В результате чего происходит портальная гипертензия,не пойму?
Почитал,как лечат портальную гипертензию:В терапии портальной гипертензии используется:
Фармакотерапия: нитраты (нитроглицерин, изосорбид), β-адреноблокаторы (атенолол, пропранолол), ингибиторы АПФ (эналаприл, фозиноприл), гликозаминогликаны (сулодексид) и др
Так это мои препараты.))) Нитраты -кординик, β-адреноблокаторы-бисопролол,ингибиторы АПФ-лозартан,даже статины если смешать с урсосаном мне в пользу,единственно аспирин меня смущает,но тут вариантов нет.
Автор: Ocean_ovna 14.09.2022 - 21:46
Нет, не совсем правильно понимаете. ПГ при НЦПГ возникает из-за микротромбозов мелких портальных вен и склероза (фиброза) портальных трактов. В дальнейшем возникают узлы регенерации без цирроза, которые сдавливают паренхиму печени, что приводит к прогрессированию ПГ. Боюсь, что СЖ здесь ни при чём... так как все вышеперечисленное происходит и у пациентов без СЖ, насколько я могу судить.
Автор: Стахий 14.09.2022 - 22:03
Читаю определение фиброза.Фиброз особое патологическое состояние, при котором происходит аномальное избыточное разрастание соединительной ткани с появлением рубцовых изменений в различных органах. Фиброз рассматривается как реакция организма, направленная на изоляцию очага воспаления от окружающих тканей и системного кровотока и препятствующая его дальнейшему распространению по организму.
Так очаг воспаления это и есть клетка печени(или любого другого органа),а у меня воспаления нету,делали гистологию (правда где-то посеяли),только дистрофические изменения.
У меня когда инфаркт был,так тоже фиброз , но там определили и по УЗИ,и по крови тропонин высокий..Но это я отвлекся,так по сердцу понятно ,сосуд перекрыт,клетки погибли,их заменила соединительная ткань.А тут же непонятно,клетки не погибли,а откуда же фиброз и склероз? По УЗИ ведь тоже все нормально!
Автор: Ocean_ovna 14.09.2022 - 22:41
Так очаг воспаления это и есть клетка печени(или любого другого органа),а у меня воспаления нету,делали гистологию (правда где-то посеяли),только дистрофические изменения.
У меня когда инфаркт был,так тоже фиброз , но там определили и по УЗИ,и по крови тропонин высокий..Но это я отвлекся,так по сердцу понятно ,сосуд перекрыт,клетки погибли,их заменила соединительная ткань.А тут же непонятно,клетки не погибли,а откуда же фиброз и склероз? По УЗИ ведь тоже все нормально!
УЗИ очень приблизительный метод обследования! но который безусловно имеет свою нишу в медицине. Склероз и фиброз развивается не за счёт гибели клеток, а за счёт гиперпродукции специфическими клетками коллагена. Гиперпродукция коллагена на месте гибели клеток - это частный случай, так сказать или один из нескольких возможных вариантов. Это ещё если очень упрощённо всё объяснять. На самом деле существует несколько типов коллагена. Коллаген может откладываться не только на месте гибели клеток, замещая их объем, но и в экстрацеллюлярном матриксе и перисинусоидальных пространствах Диссе, что в конечном итоге приводит к нарушению обмена веществ между гепатоцитами и плазмой крови, поступающей из синусоидов. Закрытие функциональных межклеточных пространств, через которые в норме осуществляются процессы обмена между гепатоцитами и кровью, поступающей по системе воротной вены, описано в литературе, как "феномен капилляризации синусоидов". Отложение коллагена в портальных трактах приводит к их фиброзу и склерозу, что также в конечном итоге нарушает внутрипеченочный кровообращение. Эти процессы и приводят к синусоидальной обструкции и портальной гипертензии. В ответ на портальную гипертензию компенсаторно, для снижения ПГ запускаются процессы шунтирования крови оттекающей из кишечника (но эта кровь содержит токсины и аммиак образующиеся в кишечнике и не обезвреживаются в печени) по анатомическим и функциональным шунтам. Токсины и аммиак попадают в том числе в головной мозг приводя к развитию клиники печеночной энцефалопатии той или иной степени выраженности. Это ещё очень упрощённо попытался объяснить, для улучшения понимания.
Автор: Стахий 15.09.2022 - 20:37
Спасибо, Вы как всегда подробны. Как страшно жить.))
Автор: Doc Martin 5.10.2022 - 20:55
Интересное фото сопровождающее статью посвященную вишнёвым ангиомам или сенильным ангиомам привлекло моё внимание. Статью писал явно врач-дерматолог. Не буду ее пересказывать. Кто хочет прочитать, вот ссылка https://acadderm.com/cherry-angioma-senile-angioma/ Кроме множества самих ангиом лоцирующихся на груди и животе, обращает на себя внимание явная гинекомастия и визуализируются подкожные вены живота, что наводит на мысль о вероятной портальной гипертензии. Если предположить, что связь между вишнёвыми ангиомами и портальной гипертензией существует, то вероятный механизм образования вишнёвых ангиом можно объяснить, например, не только повышением портального давления и коллатерализацией кровотока через подкожные вены живота, но и, возможно, гормональным дисбалансом и действием эстрогенов на фоне печеночной патологии. Связь вишневых ангиом с панкреатитом, на мой взгляд, скорее всего случайная. По крайней мере, нужны дополнительные наблюдения, чтобы исследовать причины их появления.
Автор: Ocean_ovna 13.12.2022 - 22:22
Мотивацией для написания данного поста стали не совсем однозначные (или совсем неоднозначные) оценки, которые применяются к отношению Де Ритиса (АСТ/АЛТ). Почему то укоренилось в медицинской среде твёрдое мнение (интересно, кто был тот самый первый нехороший человек, за которым потянулся шлейф последующих, вероятно ошибочных, выводов?), что отношение АСТ к АЛТ играет диагностическое значение только тогда, когда сами уровни АЛТ и АСТ выходят за пределы нормы или по научному - референсного интервала. Со временем это утверждение перекочевало от врачей к пациентам и теперь уже, при мощной народной поддержке, обрело всю силу непререкаемой истины и даже в русскоязычной статье Википедии об отношении Де Ритиса можно прочитать ту же самую информацию. Что же это за странное отношение такое? Почему оно начинает работать только тогда, когда абсолютные величины его составляющие превышают "норму", а до этого момента оно может прыгать, бегать, кувыркаться и никому до него дела нет. Мне даже кажется, что у него есть "сознание" и оно, хитрое, догадывается, что "до" можно всё что угодно, а вот если "после" - то его могут наругать, поставить на вид и в угол, в общем наказать. И почему оно работает в одних условиях, но в тех же самых условиях при включенном свете работать категорически отказывается? Капризное какое. Давайте попробуем разобраться, всё же, в чём тут дело и где зарыта та самая собака, которая покусала всех, но не тронула одного господина Де Ритиса.
Из уроков математики средней школы мы, особенно те, кто не прогуливал те самые уроки, прекрасно знаем, что при делении одного числа на другое мы находим, во сколько раз одно число больше другого или, наоборот, какую часть одно число составляет от другого. В этом и есть смысл отношения двух чисел. Почему мы должны применить к отношению Де Ритиса принцип, который можно описать словами из юмористической миниатюры - "Здесь играем, здесь не играем, здесь рыбу заворачивали" для меня лично непонятно.
Чтобы понять сложные взаимоотношения трансаминаз друг с другом, нужно определиться где они находятся в организме, какую роль выполняют, почему они могут повышаться или снижаться, и что всё это может значить.
Хорошо известно что определение уровней аланинаминотрансферазы или АЛТ и Аспартатаминотрансферазы или АСТ используется для диагностики заболеваний печени практически во всех без исключения случаях. Такая привилегия для них связана с высокой органоспецифичностью по отношению к печени, причем АЛТ считается более специфичным для заболеваний печени, поскольку данный фермент преимущественно содержится в ее цитозоле. Прежде чем перейти к механизмам, будет полезно немного предыстории. Соотношение АСТ/АЛТ было впервые описано Фернандо Де Ритисом в 1957 году. Он заметил, что НИЗКОЕ (т.е. <1) соотношение было связано с острым вирусным гепатитом. В 1979 году Коэн и Каплан изучили соотношение АСТ/АЛТ и отметили, что оно больше 2 у лиц с алкогольной болезнью печени. Они также подтвердили наблюдения Де Ритиса о низком соотношении при остром вирусном гепатите. В 1967 году Harinasuta сообщил, что абсолютное значение АСТ у алкоголиков высокое. Собственно, такое объяснение сохраняется и в наше время - в норме отношение АСТ к АЛТ около 0.8- 1, при вирусных гепатитах меньше 1, при алкогольной болезни печени 2 и выше. Опять какая-то дискриминация получается, почему в одном случае болезни печени отношение АСТ к АЛТ ниже 1, а в другом случае болезни той же самой печени отношение 2 и выше, в чём тут дело? Если АЛТ является "специфическим" для печени, можно ожидать, что любой печеночный процесс приведет к низкому соотношению АСТ/АЛТ. Давайте рассмотрим некоторые возможные механистические объяснения...
Высокое соотношение АСТ/АЛТ, наблюдаемое при алкогольной болезни печени, может быть
1. результатом непропорционально высокого уровня АСТ,
2. непропорционально низкого уровня АЛТ или
3. их комбинации.
в печени есть два изофермента АСТ: цитоплазматический (цАСТ) и митохондриальный (мАСТ). 80% активности AСТ в печени человека составляет mАСТ. Алкоголь приводит к повышению mАСТ из-за повреждения митохондрий гепатоцитов т.е. воздействие алкоголя можно назвать более глубоким по сравнению с вирусным повреждением. Эксперименты на лабораторных животных также показали, что дефицит витамина В6 достоверно снижал активность АСТ и АЛТ в то время как активность их митохондриальной фракции сохранялась. При добавлении витамина В6 активность АСТ восстанавливалась до достаточного уровня в то время как АЛТ не так заметно. Добавление В6 in vitro не влияет на активность mАЛТ и mАСТ. Результаты этих
экспериментов показывают, что трансаминазы подвержены влиянию снижения содержания витамина В6 в организме, что по видимому диктует целесообразность одновременного определения с АЛТ и АСТ содержания витамина В6, для корректной оценки уровня трансаминаз.
Низкий уровень B6 наблюдается у пациентов с алкогольным гепатитом. Если дать обратно В6, АЛТ печени повышается. AST делает то же самое, но не так сильно. https://pubmed.ncbi.nlm.nih.gov/6698365/
Клиренс АСТ и АЛТ также имеет отношение к их соотношению.
* период полувыведения для АСТ = 18 часов
* период полувыведения АЛТ = 36 часов
Поскольку период полувыведения АСТ короче, соотношение АСТ/АЛТ может снижаться в течение госпитализации.
https://pubmed.ncbi.nlm.nih.gov/15208167/
С другой стороны, поскольку АСТ выводится в печени синусоидальными клетками, по мере развития цирроза клиренс может снижаться. Результат: соотношение АСТ/АЛТ увеличивается по мере развития цирроза печени; это изменение может быть замечено через годы.
Таким образом, объяснения отношения АСТ/АЛТ >2 при алкогольной болезни печени включают:
1. повреждение митохондрий, приводящее к высвобождению mAST
2. низкий уровень В6, что приводит к подавлению АЛТ
И, если присутствует цирроз:
3. снижение клиренса АСТ
Как уже описывал в начале этой темы, трансаминазы как интегральный показатель вполне могут находится в нормальном диапазоне даже при серьезном повреждении печени (циррозе) из-за отсутствия или низкой активности на момент взятия крови фонового гепатита, на фоне дефицита витамина В6, как мы только что выяснили и по причине значительного снижения общего количества гепатоцитов на фоне цирротической трансформации печени. Известно также из наблюдений, что даже однократное употребление алкоголя приводит к относительному повышению АСТ в пределах референсного интервала или незначительно его превышая по сравнению с АЛТ с соответствующим изменением отношения Де Ритиса. Примерно через 1,5-2 недели уровни трансаминаз приходят к первоначальным значениям и соотношение АСТ/АЛТ восстанавливается. Без описания химических реакций видно, что повреждение печени при воздействии алкоголя более "глубокое", на уровне митохондрий гепатоцитов, а хроническое воздействие алкоголя вероятнее всего приводит к повреждению как мембранного аппарата митохондрий, так и повреждению их ДНК, что делает невозможным процесс их нормального деления и восстановления. Высокая частота развития печеночной энцефалопатии при алкогольной болезни печени вероятнее всего связана не только с портальной гипертензией и шунтированием, но и с угнетением первых двух реакций детоксикации аммиака в орнитиновом цикле (цикла мочевины), которые проходят именно в митохондриях гепатоцитов. Таким образом, стойкое изменение соотношения АСТ/АЛТ, даже если трансаминазы находятся в пределах референсного интервала, выглядит весьма подозрительным, особенно если у пациента в анамнезе присутствует фактор хронического употребления алкоголя и это может быть одним из немногих полезных ранних предупреждающих признаков алкогольной болезни печени до появления симптомов.
Автор: Ocean_ovna 14.12.2022 - 20:04
Очень интересная статья о лекарственных повреждениях печени по этой ссылке https://umedp.ru/articles/lekarstvennoe_povrezhdenie_pecheni_indutsirovannoe_priemom_vitaminov_a_i_e.html
из которой можно сделать вывод, что здоровый образ жизни нужно вести с умом.
Автор: Ocean_ovna 21.01.2023 - 13:08
Интересная обобщающая статья в WIKI об НРГ. На что бы обратил внимание в качестве факультативных "красных флагов", это возможные изменения биохимических показателей при НРГ - повышение уровня Щелочной фосфатазы (в 25% случаев НРГ) и снижение уровня витамина В12, а также "мерцание" уровня трансаминаз АЛТ/АСТ - чередование эпизодов их незначительного повышения с последующей самостоятельной или "псевдотерапевтической" нормализацией (после курса к.л.гепатопротектора, просто из-за совпадения этой нормализации во времени), аномальное соотношение АСТ/АЛТ. По опубликованным данным, НРГ обнаруживается при биопсии в 15% случаев повышения трансаминаз неясного генеза.
https://www.wikidoc.org/index.php/Nodular_regenerative_hyperplasia#:~:text=NRH%20is%20a%20rare%20disease,0.34%20cases%20per%20100%2C000%20individuals.
Автор: Doc Martin 23.01.2023 - 21:32
По поводу интерпретации соотношения деРитиса (АСТ/АЛТ) можно прочитать в этой статье https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3866949/.
И хотя "копья" продолжают ломать насчёт информативности и корректности подсчёта коэффициента при нормальных уровнях трансаминаз, но есть мнение что соотношение можно и нужно оценить, даже если АЛТ и АСТ в пределах нормы Поделите значение АСТ на АЛТ. Если вы получите число меньше 0,8, вы можете с большой долей вероятности сказать, что у вас нет тяжелого фиброза и цирроза печени. То есть "в идеале", даже если трансаминазы находятся в пределах референсного интервала АЛТ должен быть немного выше АСТ. Иными словами, если коэффициент меньше 0,8, то можно с уверенностью сказать, что выраженного фиброза нет. Если коэффициент более 0,8, то нельзя с уверенностью говорить об отсутствии выраженного фиброза и для подтверждения/опровержения его стадии необходимо использовать другие методы обследования. На практике, к сожалению, насколько могу судить, этому мало уделяют внимание.
- "Трансаминазы в норме? В норме. Ну и чего пристали? Не мешайте работать, пациент.)))
Хотя на этот счёт существуют очень четкие рекомендации EASL, принадлежностью к которой так любят козырять отечественные гуру гепатологии.
Распространенность выраженного фиброза одинакова у пациентов как с нормальным, так и с высоким уровнем печеночных ферментов. В связи с этим Европейская ассоциация по изучению печени (EASL) предложила следующий алгоритм скрининга:
"Рассчитайте индекс FIB-4 с помощью онлайн-калькулятора. Если результат больше 1,3 (то есть нельзя исключить выраженный фиброз), необходимо провести ультразвуковую эластографию/фиброскан печени для уточнения стадии. Достаточно четкие рекомендации, как по мне.
Калькулятор для расчета FIB-4 https://www.mdcalc.com/calc/2200/fibrosis-4-fib-4-index-liver-fibrosis
Автор: Ocean_ovna 11.02.2023 - 18:47
[i]"Рассчитайте индекс FIB-4 с
Калькулятор для расчета FIB-4 https://www.mdcalc.com/calc/2200/fibrosis-4-fib-4-index-liver-fibrosis
Думаю, с расчетом FIB4, который валидирован для вирусного гепатита С и неалкогольной жировой болезни печени (НАЖБП), тоже не все так однозначно и вероятность того, что значительная часть пациентов имеют выраженный фиброз, не говоря уже об НЦПГ/НРГ, при "нормальных" значениях FIB4, как впрочем и других расчетных индексов фиброза, остается довольно высокой. Кажется, даже при минимальных подозрениях, нужно использовать все доступные методы диагностики по максимуму... Как правило, у пациентов с НАЖБП уровень АЛТ в плазме крови выше, чем АСТ, однако при выраженном фиброзе соотношение АСТ/АЛТ превышает 1. Это соотношение имеет хорошую отрицательную прогностическую ценность и может быть использовано для исключения наличия фиброза.
Информативная статья о преимуществах и безопасности длительного лечения печеночной энцефалопатии (ПЭ) рифаксимином.
https://aasldpubs.onlinelibrary.wiley.com/doi/10.1002/hep.31708
UPD: А также обзор Cochrane об использовании пробиотиков для людей с печеночной энцефалопатией.
https://www.cochrane.org/ru/CD008716/LIVER_probiotiki-dlya-lyudey-s-pechenochnoy-encefalopatiey
По сравнению с плацебо или отсутствием вмешательства, пробиотики, вероятно, улучшают восстановление и могут привести к улучшению в развитии выраженной печеночной энцефалопатии, качества жизни и плазменных концентраций аммиака, но могут и привести лишь к небольшой разнице в смертности или не привести в разнице в смертности...
Автор: Doc Martin 27.02.2023 - 22:53
В последние годы периодически появляются научные статьи о возможности обpaтимости в некоторых случаях фиброза и даже цирроза печени при элиминации этиологического фактора ( алкоголь, гепатиты В и С). Причем это подкрепляется даже повторными гистологическими исследованиями биоптатов печени. Скорее авторы пытаются выдать желаемое за действительное, так как даже алкогольный фиброз (особенно перивенулярный) в настоящее время считается необратимым состоянием. Как правило, алкогольный фиброз представлен различными типами фиброза одновременно с преобладанием того или иного его гистологического варианта.
Хочу представить изображение гистологических препаратов в одной из статей и по возможности разобраться что же на самом деле на них зафиксировано. На прикреплённом изображении представлены гистологические препараты печени взятые методом пункционной биопсии печени у одного и того же пациента с диагностированных циррозом алкогольной этиологии через определенные длительные промежутки времени. Гистологические образцы были окрашены гематоксилином-эозином (H&E), они представлены на изображении слева, и окрашенные для выявления ретикулиновых волокон или коллагена 3 типа (reticulin stain), на изображении представлены справа. Хорошо прослеживается позитивная динамика гистологических изменений, однако несмотря на то что септы стали практически не видны при окрашивании H&E, при окраске ретикулиновых волокон они все ещё хорошо визуализируются, хотя стали заметно тоньше и местами неполными, то есть в данном случае корректнее было бы эти изменения описывать как трансформацию цирроза печени алкогольной этиологии в неполный септальный цирроз. Если сравнить препараты окрашенные H&E посередине и внизу, то отчётливо видно уменьшение расширения синусоидов, что может свидетельствовать об уменьшении степени выраженности перисинусоидального фиброза и снижении портальной гипертензии. Несмотря на такие позитивные гистологические признаки цирроз, тем не менее, остался, хотя может быть неправильно интерпретирован даже опытным патологом как препарат здоровой печени или в крайнем случае умеренный портальный фиброз, если не будет дополнительно применена окраска ретикулиновых волокон - только в этом случае диагноз цирроза печени становится однозначным и очевидным. Теперь наглядно понятно, что даже фибросканирование или эластография проведенные в динамике у такого пациента дадут снижение плотности печени ниже диапазона отсечки для цирроза печени (12-13кПа) и опять же будут неправильно интерпретированы как "умеренный фиброз" (F1-F2) или даже F0. Естественно, что публикации таких данных должны мотивировать пациентов к полному воздержанию от алкоголя или своевременному лечению гепатитов, так как это может существенно замедлить прогрессию этих заболеваний даже на цирротической стадии и увеличить ожидаемую продолжительность их жизни.
Автор: Ocean_ovna 9.03.2023 - 19:58
Пациентка из Румынии, 42 года. В 14 лет перенесла гепатит неясной этиологии (со слов пациента), изредка курит, употребляла алкоголь в умеренных дозах. Около года назад отмечает начало манифестации симптомов в виде выраженной слабости, немотивированной потери веса, бессонницы, мышечных подергиваний и спазмов, постоянного сладко-солоноватого привкуса во рту, изменение вкуса табачного дыма, усиление пигментации кожи, выраженного снижение аппетита, периодической тошноты, "мозгового тумана", затуманенного зрения, головокружения. Пациентка заподозрила у себя заболевание печени, по поводу чего неоднократно консультировалась на родине и в Италии. Патология печени всеми консультантами отвергалась. Проведенные визуализирующие методы обследования (УЗИ, МРТ, КТ) не показали никаких отклонений, признаки портальной гипертензии не выявлены. Фибросканирование печени 5.6 кПа. Биохимия крови показала снижение уровня ферритина, повышенный уровень аммиака, креатинин и мочевина на верхней границе нормы, остальные показатели в том числе LFT в пределах референсного интервала, тромбоциты 440. На коже шеи, груди и живота визуализируются (по фото) единичные капельные ангиомы (симптом Тужилина), которые обычно связывают с хроническим панкреатитом (по моему мнению капельные ангиомы характерных локализаций могут быть аналогом паукообразных ангиом и тогда они связаны с портальной гипертензией).
В мае 2022 года в румынской клинике пациентке проведена пункционная биопсия печени.
"Пункция биопсии печени
Цилиндрический фрагмент биопсии ткани печени длиной 2 см, состоящий из ткани печени с сохраненной архитектурой, некоторые портальные тракты с легким фиброзом, без выраженных воспалительных элементов, с явлениями слабовыраженного холестаза в гепатоцитах вокруг центролобулярной вены. Отсутствие признаков стеатоза. Без гранулематозных элементов. Без опухолевых элементов.
Отрицательное окрашивание по Перлс.
ЗАКЛЮЧЕНИЕ: Фрагмент биоптата ткани печени без выраженных гистопатологических изменений.
Элементов злокачественности нет.
Соотнесите с клиническими аспектами и аспектами визуализации".
Стоит отметить, что гистологические образцы в этом случае окрашивались только гематоксилином-эозином и Perls (окраска на гемосидерин). Окраска на ретикулиновые волокна не проводилась из-за странного обоснования - "отсутствии такой необходимости".
Ввиду отсутствия проблем с печенью по биохимическим данным, визуализирующим методам обследования и результатам гистологии, состояние пациентки ошибочно интерпретировано как психосоматическое расстройство (это несмотря на высокий уровень аммиака (152!!! мкмоль/л)). Ей рекомендован прием амитриптилина и наблюдение у ....психиатра
Пациентке дистанционно рекомендовано воздержаться от приема амитриптилина, начать лечение направленное на снижение уровня аммиака (лактулоза, рифаксимин, LoLa (Hepa-Merz)) и получить "второе мнение" по результатам проведенной гистологии в отделении патологии университетской клиники г. Левен (Бельгия). Для повторной оценки в отделение патологии пациенткой пересланы гистологические препараты и парафиновый блок (с целью возможности дополнительного окрашивания). В результате лечения пациентка отметила некоторое улучшение самочувствия. "Второе мнение" по гистологии печени интерпретировано как узловая регенеративная гиперплазия печени/нецирротическая портальная гипертензия и гепатопортальный склероз. В настоящее время пациентка собирается обратиться к специалисту специализирующемуся по сосудистым заболеваниям печени из группы экспертов VALDIG во Франции для выработки дальнейшей стратегии.
Скачать гистологический отчёт https://wdfiles.ru/f17c7b
Для скептиков терапевтической эффективности применения LoLa (Гепа-Мерц) хочу продемонстрировать два снимка рук румынской пациентки до и после применения Гепа-Мерц с интервалом в две недели. До начала приёма LoLa пациентка постоянно принимала рифаксимин 1200мг в сутки и лактулозу 30мл 3 раза в день с июля прошлого года. Стул был 1 раз в день, в связи с чем дозу лактулозы было рекомендовано увеличить до 60мл 3 раза в день для получения 2-3 испражнений в сутки и начать прием LoLa (Гепа-Мерц) по 1 Саше 3 раза в день. На 4й день от начала коррекции лечения пациентка отметила значительное улучшение самочувствия, уменьшился неприятный запах от тела и фекально-сладкий привкус во рту, значительно улучшился сон, который до этого был очень поверхностный и прерывистый.
Ссылка для скачивания фото
https://fv2-1.failiem.lv/down.php?i=s2hhxw3uz&view
Клинический анализ крови до коррекции лечения
https://fv2-1.failiem.lv/down.php?i=ym34gn9ps&view
Обратите внимание на определенный нормальный уровень аммиака и тем не менее явные внешние признаки тяжёлой интоксикации организма, а также на изменённое соотношение АСТ/АЛТ=1.5 и парадоксально нормальный как для общепринятых взглядов в гепатологии при диффузных заболеваний печени уровень тромбоцитов!
Автор: Ocean_ovna 17.04.2023 - 21:14
Информативная англоязычная статья о гипераммониемии - Гипераммониемия - метаболическое состояние, характеризующееся повышенным уровнем аммиака, азотсодержащего соединения. Аммиак является сильным нейротоксином. Гипераммониемия чаще всего проявляется неврологическими признаками и симптомами, которые могут быть острыми или хроническими, в зависимости от основной патологии. Гипераммониемию следует распознать на ранней стадии и немедленно лечить, чтобы предотвратить развитие опасных для жизни осложнений
https://www.ncbi.nlm.nih.gov/books/NBK557504/
И ещё одна статья на английском - Пациенты с общим вариабельным иммунодефицитом (ОВИН) подвержены развитию синдрома заболевания печени, известного как узловая регенеративная гиперплазия (NRH). Целью данного исследования было определение характеристик и течения этого осложнения ОВИН.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3731765/
Для правильной диагностики и подозрении на ОВИН важен корректный сбор анамнеза жизни пациента. Обычно пациент указывает на частые инфекционные процессы различных локализаций. Частые и необычные инфекции могут впервые возникнуть в раннем детстве, в подростковом возрасте или у взрослых людей. У большинства пациентов это состояние диагностируется лишь в возрасте 20-40 лет.
Эта форма иммунодефицита встречается относительно часто, в связи с чем в ее названии есть слово ?общая?. Степень и тип недостаточности иммуноглобулинов в сыворотке крови, а также клиническое течение у разных пациентов различны, что объясняет наличие слова ?вариабельная?.
Общая вариабельная иммунная недостаточность (ОВИН) - нарушение, характеризующееся низкими уровнями иммуноглобулинов (антител) в сыворотке крови и повышенной чувствитель-ностью к инфекциям. У некоторых пациентов имеется снижение таких иммуноглобулинов, как IgG и IgA. У других могут быть снижены уровни всех трех основных видов иммуноглобулинов (IgG, IgA и IgM). Основным проявлением ОВИН у большинства пациентов являются рецидивирующие инфекции уха, придаточных пазух, носа, бронхов и легких. примерно у 20% иммунная недостаточность впервые обнаруживается как значительное снижение количества тромбоцитов в крови или даже тяжелая анемия в связи с разрушением красных кровяных клеток. Аутоантитела могут также вызвать артрит или эндокринные нарушения, например, заболевание щитовидной железы.
У некоторых больных ОВИН возникают жалобы на желудочно-кишечные расстройства, например, боль в животе, повышенное газообразование, тошноту, понос и снижение веса тела. Диагноз подтверждается обнаружением низких уровней иммуноглобулинов, в том числе IgG, IgA и обычно IgM. У пациентов, полностью иммунизированных против полиомиелита, кори, дифтерии и столбняка, антитела к одной или нескольким из этих вакцин могут иметь очень низкие уровни или отсутствовать.
Автор: Ldof 10.10.2023 - 16:57
По поводу Буеверова Алексея Олеговича, кто-нибудь попадал к нему на прием? Просто планировал ехать в Москву специально, очень затратно все это будет. А отзывов очень много негативных, вообще не понимаю как-так, какой то диссонанс.
Автор: ama7ed 11.10.2023 - 15:49
На прием не попадал, но смотрел очень много информации и роликов в интернете. Довольно грамотный специалист, много умных факторов разъясняет.
Автор: Ocean_ovna 25.12.2023 - 23:14
Мы никогда не говорим о субклинических последствиях повреждения печени. Миллионы людей страдают заболеваниями печени без симптомов.
Вопрос, который мы должны задать, заключается в том, сколько людей страдают от заболеваний печени, а не от психического заболевания, которое мы предполагаем, когда видим странное поведение, но это критические случаи. В более широком смысле, как насчет людей, у которых аммиак незначительно повышен или анализ проведен некорректно на преаналитическом этапе? Многие ли из нас списывают проблемы с памятью или спутанность сознания просто на стареющий мозг, хотя на самом деле это небольшое токсичное отравление? Думаю, проблема в том, что мы не знаем. Мы не проверяем раннюю стадию заболевания печени и очень мало знаем о том, как оно на самом деле влияет на бессимптомных жертв. Мы легко предполагаем деменцию, болезнь Альцгеймера или просто нормальное старение, но почти никогда не рассматриваем заболевание печени как причинный фактор этих состояний. Возможно многие пациенты с подозрением на раннюю деменцию на самом деле являются пациентами с хроническим диффузным заболеванием печени с персистирующей формой печеночной энцефалопатии и наряду с терапией направленной на улучшение сосудистого и микроциркуляторного компонента в той же, если не в большей мере нуждаются в терапии направленной на снижение уровня аммиака и других кишечных токсинов, а определение уровня аммиака из экзотического и иногда малодоступного исследования должно превратиться в стандартную процедуру и не только для пациентов гепатологического профиля и ПЭ следует подозревать, диагностировать и активно лечить на как можно более ранних стадиях, поскольку это серьезное осложнение, приводящее к необратимому ухудшению когнитивных функций пациента и значимым социальным последствиям как для самого пациента, так и для его близких, а количество пациентов нуждающихся в такой терапии на порядки выше, чем это принято считать до сих пор в официальной медицине.
Баллы MELD (шкала для оценки терминальной стадии заболеваний печени)по-видимому, не коррелируют с тяжестью HE. Это конкретное несоответствие между тяжестью HE и оценкой MELD, по-видимому, объясняет низкие показатели трансплантации печени у этих пациентов и может способствовать высоким показателям смертности, вызванной HE. Трансплантация печени обычно излечивает HE, но HE не увеличивает показатель MELD и, следовательно, не увеличивает вероятность трансплантации печени.
Форум Invision Power Board (http://www.invisionboard.com)
© Invision Power Services (http://www.invisionpower.com)